离III期临床更近一步!自体干细胞治疗特应性皮炎的II期试验证实,可显著改善其症状
近期,《Stem Cell Research & Therapy》期刊发表了一项题为“自体脂肪干细胞治疗中重度特应性皮炎患者的疗效和安全性:一项多中心、随机、单盲、安慰剂对照的II期试验”的研究论文[1]。

该研究旨在系统评估自体脂肪组织来源的间充质干细胞(AtMSC)治疗难治性中重度AD患者的疗效与安全性。
结果表明:自体间充质干细胞疗法改善了中重度AD症状,为治疗慢性炎症性疾病提供了一种有前景的治疗选择。需要开展进一步研究,包括双盲3期临床试验,以证实这些发现并探索其他生物标志物。
特应性皮炎的疾病背景与治疗需求
特应性皮炎是一种以剧烈瘙痒、反复发作为特征的慢性炎症性皮肤病。研究显示,中重度AD除皮肤表现外,还会显著影响患者的情绪和心理健康。该病在儿童中的终生患病率达10%~20%,在成人中约为3%~7%,已成为全球公共卫生的重要负担。
AD的治疗选择依严重程度而异,中重度患者常需使用全身性免疫抑制剂,如糖皮质激素、环孢素及JAK抑制剂等,但长期应用可能带来明显副作用与毒性风险。近年来,针对特定细胞因子(如IL-4/13、IL-13、IL-31)的生物制剂为部分患者带来新希望,然而仍有相当比例患者无法实现完全或长期缓解。
间充质干细胞的治疗潜力
الخلايا الجذعية الوسيطة الوسيطة MSC (في بيولوجيا الخلية)是一类具有多向分化潜能的干细胞,可从脐带、骨髓、脂肪等多种组织中获取。其表面表达CD73、CD90、CD105等标志物,不表达造血系标志物如CD45、CD34等。
MSCs在抗炎、组织修复及免疫调节中发挥关键作用,能够通过与先天性和适应性免疫系统的互动,抑制T细胞、B细胞、树突状细胞及自然杀伤细胞等的过度活化。动物实验表明,MSCs对特应性皮炎、哮喘等过敏性疾病具有改善潜力,这些特性使其成为治疗AD等免疫相关疾病的有前景策略。
尽管已有若干临床试验探讨MSCs治疗AD的效果,但其在大规模人群中的疗效与安全性证据仍不充分。为此,研究团队开展了一项临床试验,旨在评估AtMSC治疗对114例常规治疗无效的中重度AD成人患者的疗效与安全性,并通过检测血清细胞因子水平进一步探索其作用机制。
研究方法
本研究为一项多中心、随机、单盲、安慰剂对照的II期临床试验。共纳入114例受试者,随机分配至治疗组与安慰剂组,分别接受两次静脉输注(间隔4周)。
治疗期间,每4周进行一次临床评估,主要指标包括湿疹面积与严重程度指数(EASI)、特应性皮炎评分(SCORAD)和研究者总体评估(IGA),总随访时间为16周。同时,采用酶联免疫吸附试验(ELISA)对血清中多种细胞因子进行定量分析。
结果
受试者基线特征
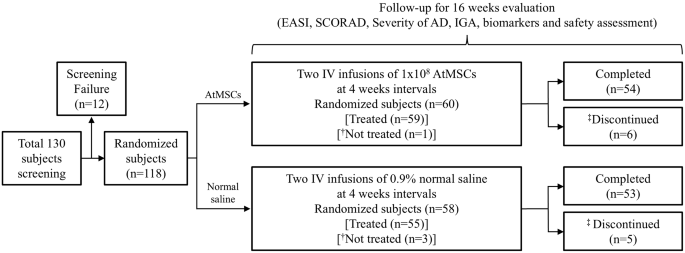
图1:临床试验中研究对象处置情况概述。
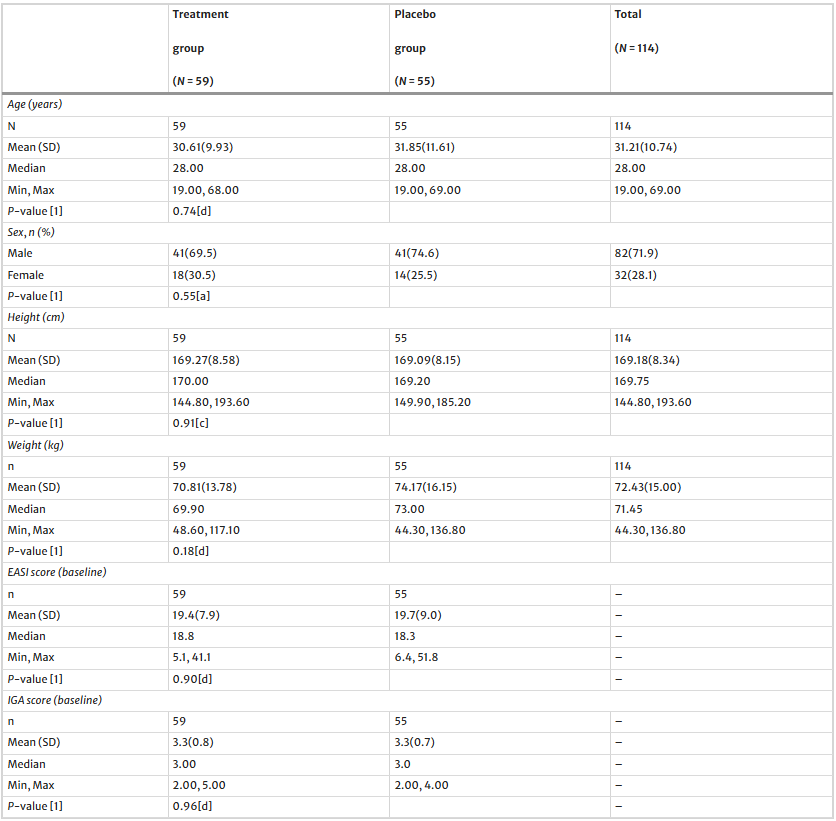
表1:人口统计信息(完整分析集)
在合并症方面,受试者中以螨虫过敏最为常见,共35例(30.7%),其中治疗组20例(占该组33.9%),安慰剂组15例(占该组27.3%)。其次为动物过敏20例(17.5%),治疗组13例(22.0%),安慰剂组7例(12.7%);过敏性鼻炎16例(14.0%),治疗组与安慰剂组各8例。其他疾病信息详见补充材料,整体合并症分布反映了受试群体中过敏性疾病较为普遍。
临床疗效结果
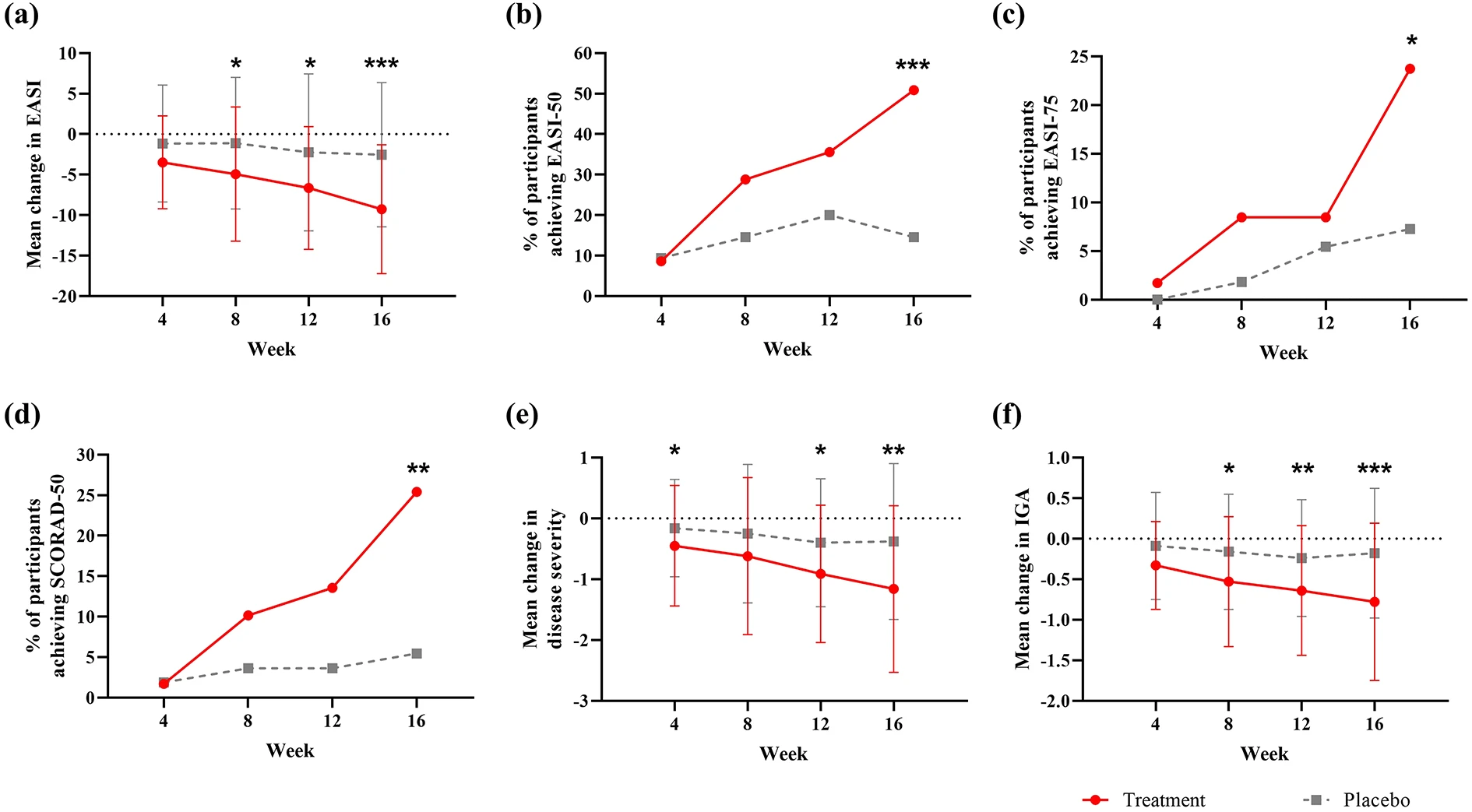
图2:aEASI总分平均变化值,b达到EASI-50的参与者百分比,c达到 EASI-75的参与者百分比,dSCORAD总分降低50%或以上的参与者百分比(SCORAD-50),e疾病严重程度平均变化值,fIGA评分平均变化值——所有指标均以各时间点的基线为基准进行测量
多维度的疾病控制效果:除EASI评分外,该疗法对患者病情的改善是全方位的。
-
SCORAD评分:变化趋势与EASI高度同步(图2d),证明了疗效在不同评价体系下的一致性。
-
IGA评分与严重程度:治疗组在研究者全球评估(IGA)及整体疾病严重程度分级上均优于安慰剂(图2e-f)。
-
局限性观察:尽管多项指标向好,但两组在SCORAD75%改善(SCORAD-75)这一严苛指标上均未达标,提示该疗效在更极端的全面清除方面仍有提升空间。
综合置信区间分析(上限低于0),这些数据一致指向治疗组的临床获益显著优于安慰剂,能够有效缓解特应性皮炎的多种症状指标。
生物标志物分析
基线时两组所有检测细胞因子水平均无显著差异。治疗过程中,IL-4、IL-5、IL-13、IL-31等Th2相关细胞因子在组间未见显著变化。然而至第16周,治疗组血清TARC(即CCL17)水平较安慰剂组显著降低(图3a–e),提示AtMSC治疗可能通过抑制Th2细胞趋化途径发挥作用。其他标志物如PGE2、ECP、TGF-β1、IL-6、IL-8等在各时间点均无组间显著差异(表2和补充表5)。
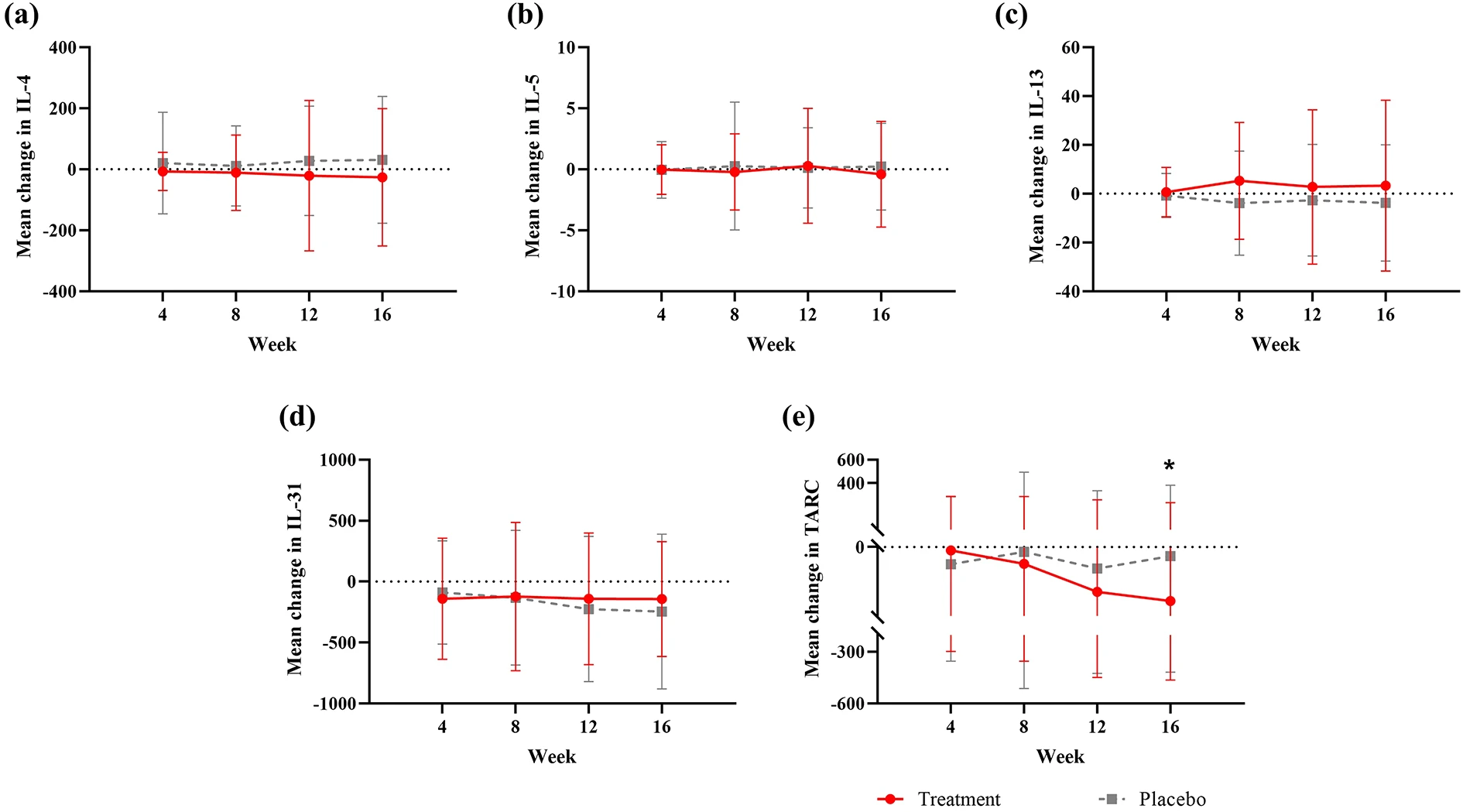
图3:各时间点血液中各因子水平较基线的平均变化
安全性评估
在安全性方面,治疗期间共29例(25.4%)患者报告43例次不良事件,其中药物相关不良反应(ADR)发生率为4.4%(5例/10例次),组间无显著差异。最常见ADR为头痛(2.6%),其余包括头晕、荨麻疹、白癜风、恶心、静脉炎等,发生率均低于1%。仅1例患者因非ADR不良事件退出研究,未发生严重不良事件(SAE)。生命体征、实验室检查及体格检查均未见具有临床意义的异常。
讨论研究的意义
第一,研究的创新性和治疗优势:本研究是首个大规模II期临床试验,证实了自体脂肪来源间充质干细胞(AtMSC)治疗中重度特应性皮炎(AD)的有效性和安全性。与安慰剂相比,AtMSC能显著降低EASI评分、SCORAD评分、疾病严重程度及研究者整体评估(IGA)评分,且未出现明显并发症。
相较于骨髓来源MSC,AtMSC更易于从患者自体脂肪组织中获取,同时因HLA配型匹配可能降低免疫排斥风险,从而在长期安全性和疗效维持方面更具潜力。
第二,作用机制与生物标志物发现:研究重点关注了AD关键生物标志物TARC(即CCL17),发现治疗组在第16周时血清TARC水平显著低于安慰剂组。TARC作为Th2细胞的强趋化因子,其降低可能抑制致病性Th2细胞向皮肤浸润,从而部分解释临床改善的机制。
然而,其他Th2相关细胞因子(如IL-4、IL-5、IL-13和IL-31)的血清水平未见显著变化,这可能由于观察时间较短、或细胞因子变化主要发生于皮肤组织层面。未来研究需直接检测组织内细胞因子,并延长随访以明确AtMSC是否影响后续细胞因子产生。
第三,疗效对比与未来研究方向:与现有AD生物制剂(如度普利尤单抗、曲罗芦单抗)和JAK抑制剂(如巴瑞替尼)相比,AtMSC在第16周达到EASI-75的应答率(23.7%)虽略低,但仍处于可比范围,提示其可作为AD临床治疗中一种有前景的替代或辅助选择。
研究也指出局限性,包括单盲设计、未检测IFN-γ和IL-17等细胞因子、评估周期仅16周等。因此,未来III期试验应采用双盲设计,延长疗效评估时间,并探索IL-17等生物标志物以优化患者筛选,从而全面评估AtMSC治疗的长期效果和复发率。
总结
综上所述,自体脂肪来源间充质干细胞(AtMSC)治疗可显著改善中重度特应性皮炎患者的临床症状,且安全性良好。其免疫调节特性为AD及其他慢性炎症性疾病提供了新的治疗思路。
此外,输注的MSCs可能在体内维持较长期疗效,支持其作为AD持久管理策略的潜力,值得进一步开展更大规模、更长随访的临床研究予以验证。
主要参考资料:
[1] Seok, J., Kim, SY., Lee, WG 等。 自体脂肪干细胞治疗中重度特应性皮炎患者的疗效和安全性:一项多中心、随机、单盲、安慰剂对照的 II 期试验。 干细胞研究与治疗 16 , 671 (2025)。https://doi.org/10.1186/s13287-025-04763-y
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。
郑重声明:本文版权归原作者所有,转载文章仅为传播更多信息之目的,如作者信息标记有误,请第一时间联系我们修改或删除,多谢。



اترك تعليقاً