真实案例!间充质干细胞治疗2型糖尿病1例:实现血糖达标、药物减量与胰岛功能改善的三重获益!

一、传统治疗的局限与人脐带间充质干细胞治疗新策略
二、脐带间充质干细胞移植治疗2型糖尿病的作用机制
三、资料与方法
研究设计与伦理规范
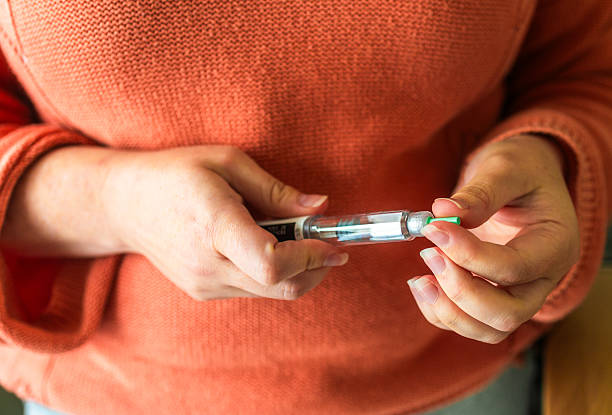
本研究为一项遵循《赫尔辛基宣言》原则的临床研究,已通过医院伦理审查委员会批准,并在中国临床试验中心完成注册。所有参与患者均签署知情同意书,确保研究符合伦理与法律规范。研究对象为一名60岁男性2型糖尿病患者,病程达20年,伴有高血压、脂肪肝及糖尿病视网膜病变1期,且既往胰岛素联合口服药治疗下血糖控制不佳(HbA1c 8.5%),于2022年6月在北京大学深圳医院内分泌科接受人脐带间充质干细胞(hUC-MSCs)治疗。
干细胞制备与质量控制
所使用的hUC-MSCs注射液由北科生物科技公司(深圳)提供。细胞来源于足月胎儿脐带,通过组织块贴壁法分离培养,获取第2‑4代细胞。制备过程包含系统性质量检测:HLA分型、表面标志物鉴定、三系分化能力验证、端粒酶活性、甲基化状态、核型分析、癌基因/抑癌基因检测及病原学筛查。合格细胞经程序降温后冻存于‑196°C液氮,临床使用前经复苏、洗涤、质检及重悬,全程在12小时内完成,符合国际细胞治疗学会(ISCT)质量标准。
治疗方案与观察流程
研究设定了8周的药物稳定筛查期,基线评估后对患者进行hUC-MSCs静脉输注,剂量为1×10⁶cells/kg/次,每周1次、连续3周。每次输注后住院观察24小时。随访时间点包括治疗结束时(W0)及输注后第1、2、3、4、12周,允许±3天的弹性访视窗。研究期间患者维持标准化饮食与运动,并根据指南动态调整降糖方案,控制目标为空腹血糖4.4–7.0mmol/L、餐后血糖4.4–10mmol/L,预设胰岛素与口服药的减停条件。
结局评估指标
有效性评估涵盖血糖相关指标(空腹血糖、餐后2小时血糖、糖化血红蛋白)、C肽水平(空腹及餐后2小时),以及通过稳态模型计算的胰岛素抵抗指数(HOMA-IR)和胰岛β细胞功能指数(HOMA-β)。安全性评估系统记录所有不良事件,包括输注相关反应(生命体征异常、过敏、发热等)、实验室指标异常(肝肾功能、凝血、血常规等)、影像学检查结果,并特别监测严重不良事件(如严重低血糖、新发感染、恶性肿瘤或死亡)。
四、结果
有效性
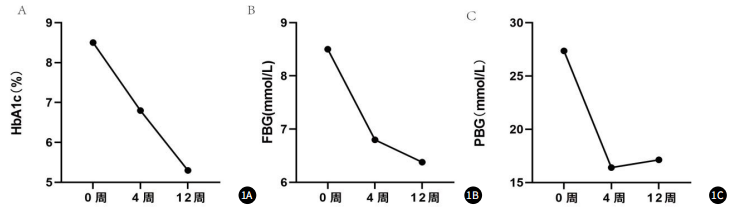
图1:随访期间血糖控制情况。注:图1A:W0 与 W4、W12 的 HbA1c 水平的变化;图1B:W0 与 W4、W12 的 FBG 水平的变化;图1C:W0 与 W4、W12 的 PBG 水平的变化。
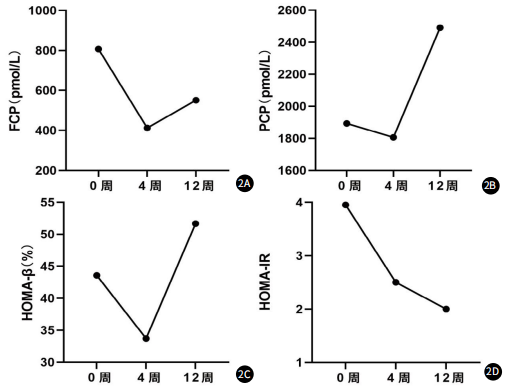
图2:随访期间胰岛情况。注:图2A:W0与W4、W12的FCP水平的变化;图2B:W0 与 W4、W12 的 PCP水平的变化;图2C:W0 与 W4、W12 的 HOMA-β 水平的变化;图2D:W0 与 W4、W12 的 HOMA-IR 的变化。

safety
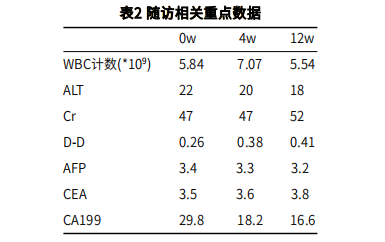
五、四大方面讨论脐带间充质干细胞移植治疗2型糖尿病的有效性
01、显著改善血糖控制,疗效与传统药物相当
糖化血红蛋白 (HbA1c) 作为评估2~3个月平均血糖水平的关键指标,能有效反映长期血糖控制状态,是本研究的核心疗效观察终点。
Li Zang等开展的 Ⅱ 期随机双盲对照试验 (n=91) 表明:接受3次UC-MSCs静脉输注的治疗组 (n=45),其HbA1c水平在移植后第9周出现最大幅度下降,虽在20、32及48周随访时小幅回升,但仍显著低于基线值。该趋势与 Lian 团队的研究结果一致:16 例接受hUC-MSCs治疗 (1×10⁶cells/kg/周×3周) 的患者,在第84±3天时 HbA1c 显著降低,且空腹血糖 (FBG) 呈持续下降趋势。
本案例中患者 HbA1c 动态变化与上述研究高度吻合,证实静脉输注hUC-MSCs能持续改善T2DM患者的HbA1c及FBG水平。值得注意的是,该疗法达到的HbA1c降幅与传统降糖药物相当,进一步支持hUC-MSCs治疗T2DM的潜在临床价值。目前一般认为细胞治疗代谢周期为3~6 月,从本例患者的 HbA1c及FBG来看,患者12周前持续下降,考虑静脉输注hUC-MSCs起到降糖作用,说明静脉输注hUC-MSCs前期作用明显,但目前尚未有大型研究静脉注射hUC-MSCs的最佳剂量、次数及最佳间隔时长等,未来仍需要更多的临床试验来研究hUC-MSCs相关的临床使用问题。
02、可能改善胰岛β细胞功能,效果呈现延迟性
除了降糖,hUC-MSCs治疗还可能通过多种机制改善胰岛β细胞功能。动物实验表明,其可促进β细胞增殖、改善自噬、调节局部免疫微环境。在本案例中,这一改善作用并非立竿见影,患者反映β细胞功能的空腹C肽和餐后C肽水平在治疗4周后才开始持续上升至12周,提示hUC-MSCs对胰岛功能的修复作用可能是一个相对缓慢的过程。
03、通过多靶点机制有效改善胰岛素抵抗
胰岛素抵抗是2型糖尿病的核心病理环节,而hUC-MSCs被证实能多途径改善这一状态。其机制包括激活关键的胰岛素信号通路(如IRS1/Akt)、抑制NLRP3炎症小体介导的慢性炎症,以及调控肝脏糖异生关键酶的表达。本案例中患者的胰岛素抵抗指数在随访期间持续低于基线,并在12周时降至最低,为hUC-MSCs改善人体胰岛素抵抗提供了直接的临床证据The
04、有助于减少外源性降糖药物依赖,但疗效存在异质性
临床研究显示不同输注方案下UC-MSCs对T2DM的疗效存在差异:一项采用静脉联合胰腺血管内注射 (间隔5天) 的研究表明,治疗6个月后患者HbA1c及胰岛素用量显著下降 (41%实现胰岛素撤除,29%减量≥50%),但疗效在后续3~6个月内逐渐减退。与之对比,18例接受三次静脉输注 (间隔2周) 的患者中,6个月随访时仅8例表现为空腹及餐后血糖下降,且胰岛素用量无统计学差异。另有试验对6例患者实施两次静脉输注 (间隔2周),在≥24个月随访期内3例于25~43个月间完全停用胰岛素,其余患者虽需持续注射但剂量减少。综合表明UC-MSCs治疗T2DM具有潜在临床价值,但各研究中胰岛素需求改善程度及维持时长存在显著异质性。
在本病例中,患者输注hUC-MSCs后实现缓慢减药,到第四周实现了减停口服降糖药物,到 4 周胰岛素用量较基线胰岛素用量下降 > 50%。hUC-MSCs 治疗降低 T2DM 患者外源性胰岛素需求的潜在机制具有多靶点特性:
- 一方面通过归巢效应定向迁移至受损胰腺组织,分化为胰岛素生成细胞 (IPCs) 并促进局部组织修复;
- 另一方面分泌抗炎因子与免疫调节因子,通过旁分泌途径改善胰岛微环境。同时可能通过三重协同作用减少降糖药物依赖:缓解 β 细胞功能障碍、增强胰岛 β 细胞保护效应、系统性改善胰岛素抵抗状态。
六、讨论脐带间充质干细胞治疗2型糖尿病的安全性
七、结论
郑重声明:本文版权归原作者所有,转载文章仅为传播更多信息之目的,如作者信息标记有错误,请第一时间联系我们修改或删除,多谢。



Leave a Reply