美国细胞疗法:近30款产品上市,多维适应症下的研发格局与生态解码
图源:AI生成
美国上市细胞疗法及相关法规概述
目前美国市面上销售的细胞治疗产品近30种,包括19种体细胞疗法和9种干细胞疗法。其中,15种为自体疗法,13种为异体疗法。此外,12种为基因改造疗法,16种为非基因改造疗法(表1)。
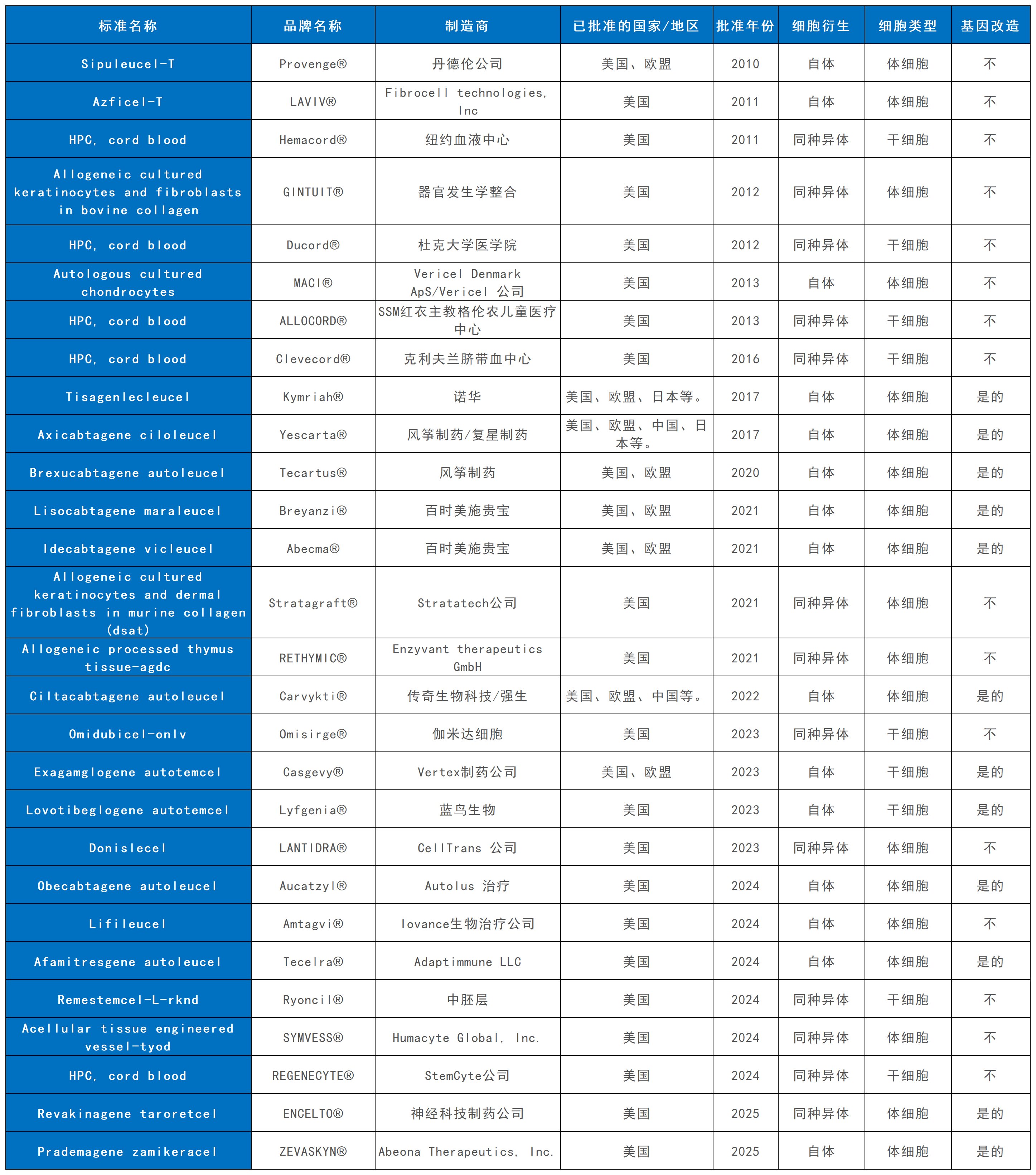
表1:美国批准的细胞疗法产品。
2010年,美国食品药品监督管理局(FDA)批准了首个细胞治疗产品Sipuleucel-T(商品名Provenge®)。Sipuleucel-T是一种于2010年在美国获批的治疗性癌症疫苗,临床试验表明其能显著提高患者的生存率。接受Sipuleucel-T治疗的无症状或轻微症状的转移性去势抵抗性前列腺癌患者,其3年生存率比接受安慰剂的患者高出10%,开启了细胞疗法商业化的先河。
一、造血干细胞疗法:基因编辑时代的疗效确证
美国在造血干细胞领域不仅布局最早,更通过基因编辑技术实现了疗效的质的飞跃。
Casgevy®(exagamglogene autotemcel)作为全球首款获批的CRISPR基因编辑疗法,其临床数据展现出卓越的疗效持久性。针对12岁及以上镰状细胞病患者的关键III期试验显示,在44名接受治疗的患者中,30名完成充分随访的患者里有29名(97%)在至少连续12个月内未发生血管闭塞危象,且所有30名患者在同一时期内均未因VOC住院治疗。
最新公布的长期随访数据进一步证实了疗效的稳定性:截至2025年4月,45例12岁以上患者全部达到VF12终点(连续12个月无VOC),平均无VOC持续时间达35.3个月;在输血依赖型β-地中海贫血患者中,55/56例(98.2%)实现TI12终点(连续12个月脱离输血),平均脱离输血时间达41.4个月。更令人振奋的是,针对5-11岁儿童患者的首次临床数据显示:4例SCD患儿全部达到VF12,且无一例在输注后出现VOC;6例TDT患儿全部达到TI12,13例患儿中有12例已脱离输血,最长脱离时间近两年。
Lyfgenia®(lovotibeglogene autotemcel)在2023年获批时提交的临床数据显示,47例接受治疗的患者中,33例可进行疗效评估,其中30例在输注后6-18个月内实现VOC和严重VOC完全缓解。所有33例患者的溶血标志物均接近正常水平,患者报告的疼痛强度和疲劳等症状持续改善。
Omisirge®(omidubicel-onlv)的临床数据也在不断拓展。2023年获批用于血液系统恶性肿瘤时,一项纳入36例患者的美国研究显示,移植后100天和365天的无病生存率分别为95.2%和82.5%,总生存率分别为96.3%和84.2%。
2025年12月,该产品新增重型再生障碍性贫血适应症,基于美国国立卫生研究院领衔的单中心研究:患者中性粒细胞恢复中位时间仅11天,86%在100天内实现早期且持续的中性粒细胞重建,86%摆脱红细胞输注依赖,未观察到重度急慢性GVHD,疾病无进展生存率和总生存率均高达92%。
二、CAR-T疗法:从血液瘤到多线治疗的纵深推进
美国已批准的7款CAR-T产品构成了全球最完备的治疗矩阵,临床数据持续积累。
Kymriah®(tisagenlecleucel)作为全球首个获批的CAR-T疗法,其长期随访数据验证了治愈潜力。最初59例复发/难治性淋巴细胞白血病患者中,输注1个月后总缓解率达93%。3年随访研究显示,无进展生存期和总生存期分别为44%和63%。首例接受治疗的6岁患儿在10年随访期内未复发,成为CAR-T疗法实现临床治愈的标志性案例。
Yescarta®(axicabtagene ciloleucel)在101例难治性大B细胞淋巴瘤患者中,客观缓解率达82%,完全缓解率54%,18个月总生存率为52%。
Carvykti®(ciltacabtagene autoleucel)作为中美合作的典范,在复发/难治性多发性骨髓瘤治疗中展现出惊艳数据:客观缓解率97.9%,完全缓解率82.5%,27个月无进展生存率和总生存率分别达54.9%和70.4%。
Aucatzyl®(obecabtagene autoleucel)的获批标志着CAR-T向安全性优化的方向演进。其临床试验中,≥3级细胞因子释放综合征发生率仅2.4%,≥3级免疫效应细胞相关神经毒性综合征发生率7.1%,支持门诊治疗的可行性。
三、TIL疗法:实体瘤治疗的里程碑突破
Amtagvi®(lifileucel)作为全球首个获批的TIL疗法,为实体瘤细胞治疗开辟了新路径。FDA批准所基于的II期C-144-01研究中,73例接受FDA批准剂量范围治疗的患者(主要疗效队列),客观缓解率为31.5%(95%CI: 21.1%-43.4%),其中完全缓解3例(4.1%),部分缓解20例(27.4%)。中位缓解持续时间尚未达到(95%CI: 4.1个月-未达到)。在23例应答者中,56.5%、47.8%和43.5%分别在6、9和12个月时维持持续缓解。
2026年公布的真实世界数据进一步印证了其临床价值。41例在授权治疗中心接受商业Amtagvi治疗的可评估患者中,经医生确认的客观缓解率达44%(18/41),疾病控制率为73%(30/41)。值得注意的是,接受过两线或更少治疗的患者ORR高达52%(12/23),显著高于接受三线及以上治疗患者的33%(6/18)。这提示早期使用可能带来更优获益。
四、TCR-T疗法:靶向胞内抗原的新维度
Tecelra®(afamitresgene autoleucel)作为全球首个获批的TCR-T疗法,靶向MAGE-A4抗原,为滑膜肉瘤患者带来新希望。
关键II期SPEARHEAD-1研究(队列1)纳入52例接受过中位三线治疗的滑膜肉瘤(44例)和黏液样/圆细胞型脂肪肉瘤(8例)患者。中位随访32.6个月时,滑膜肉瘤患者的客观缓解率达39%(17/44),中位缓解持续时间11.6个月,中位总生存期尚未达到。
FDA官方披露的数据显示,总体客观缓解率为43.2%,中位至缓解时间4.9周,中位缓解持续时间6个月。在应答者中,45.6%和39.0%的缓解持续时间分别达到≥6个月和≥12个月。
五、胰岛细胞疗法:1型糖尿病的功能性治愈
Lantidra®(donislecel)作为首款获批的同种异体胰岛细胞疗法,为脆性1型糖尿病患者提供了摆脱胰岛素依赖的可能。关键临床试验显示,70%的患者在输注后1年实现完全胰岛素独立,34%的患者在5年时仍维持胰岛素独立状态。
一项对30例患者的研究中,19例在末次移植后1年内糖化血红蛋白≤6.5%且未发生严重低血糖事件,20例在末次移植后1年内无需胰岛素治疗,部分患者维持良好血糖控制长达6年。
六、创新细胞疗法前沿进展
Orca-T作为一种高精度T细胞免疫疗法,其关键III期Precision-T研究结果显示,与传统异基因造血干细胞移植相比,Orca-T在无中重度慢性移植物抗宿主病生存率方面具有统计学显著且临床意义的改善。1年时,Orca-T组无中重度cGvHD生存率为78%,而对照组为38%;总生存率分别为94%与83%;中重度cGvHD累积发生率分别为13%与44%。该产品的BLA已获FDA受理并授予优先审评资格。
七、间充质干细胞疗法:零的突破
Ryoncil®(remestemcel-L-rknd)于2024年12月获批,成为美国首个获批的间充质干细胞疗法,填补了该领域长达十余年的空白。该产品由Mesoblast公司开发,用于治疗2个月及以上儿科患者的类固醇难治性急性移植物抗宿主病(SR-aGVHD)。
临床疗效基于一项多中心、单臂III期研究(NCT02336230),纳入54例接受异基因造血干细胞移植后发生SR-aGVHD的儿科患者。研究结果显示,第28天总缓解率达70%,其中完全缓解率30%,部分缓解率41%。第28天达到缓解的患者,其至第100天的生存率显著高于未缓解者(87%vs47%,p=0.0001)。与匹配的历史对照组相比,Ryoncil治疗组的第28天总缓解率(70% vs 43%)和第100天生存率(74%vs57%)均显著提高。
在安全性方面,最常见的不良反应(发生率≥20%)包括感染性疾病、发热、出血、水肿、腹痛和高血压。该产品禁用于对二甲基亚砜或猪/牛蛋白已知过敏的患者。
Ryoncil的获批历程颇具波折:2019年首次提交BLA申请,因临床试验设计与生产一致性问题先后于2020年、2023年两次被驳回。最终,在申办方与FDA就补充验证性数据达成协议后,于2024年获批上市。这一案例生动诠释了FDA在保持严格证据要求的同时,通过密切沟通为企业开辟可行路径的监管智慧。
Ryoncil的获批被国际细胞与基因治疗学会誉为“间充质干细胞领域的历史性里程碑”,有望重新激发业界对MSC疗法的研发热情与投资信心。该产品目前已在美国上市并可订购。
美国细胞疗法监管框架分析:分层分类与灵活审评
美国细胞疗法监管框架的构建可追溯至1993年FDA发布的《人类细胞和组织指南》。当前,监管依据主要来自《联邦食品、药品和化妆品法案》与《公共卫生服务法案》,细胞疗法被纳入生物制品管理范畴。具体执行由FDA下属的生物制品评估和研究中心及其细胞疗法和基因疗法办公室负责。
分层分类管理是监管体系的核心特征。依据操作程度与功能用途,细胞产品被划分为351类和361类。涉及“超过最低限度操作”(如体外扩增、基因修饰)或用于“非同源用途”的产品被定义为“351类产品”,须提交研究性新药申请和生物制品许可申请,接受最严格监管。仅进行“最低限度操作”(如分离、洗涤、冷冻)且用于“同源用途”的产品则被归类为“361类产品”,享受相对宽松的监管要求。特别值得注意的是,基因改造产品无论操作程度如何,一律归入351类,受最高标准监管。
加速审评机制体现科学灵活性。美国通过《21世纪治愈法案》建立了再生医学先进疗法(RMAT)途径,允许基于II期临床试验数据进行有条件批准。这一机制在实践中展现出“标准从严、沟通从活”的特点。
以Ryoncil®为例,该产品于2019年首次提交审批申请,因临床试验设计与生产一致性问题先后于2020年、2023年两次被驳回。最终,在2023年底申办方与FDA就补充验证性临床试验方案达成协议后,于2024年获得批准。这一案例生动诠释了FDA在保持严格证据要求的同时,通过密切沟通为企业制定可行解决方案的监管智慧。
总结
纵观美国上市细胞疗法的发展历程,可归纳出三个核心特征:
一是“全”,技术谱系完整。从造血干细胞到CAR-T,从TIL到TCR-T,多元技术路径并行发展,形成互补共生的创新生态。
二是“新”,源头突破引领。全球首个基因编辑疗法Casgevy®、首个TIL疗法Amtagvi®、首个TCR-T疗法Tecelra®均率先在美国落地,彰显其基础科研转化的强大能力。
三是“广”,适应症覆盖多维。细胞疗法已从血液瘤拓展至实体瘤、自身免疫病、遗传病(如镰状细胞病、先天性无胸腺症)、退行性疾病及组织修复等多个领域,治疗边界持续外延。
美国之所以能持续引领全球细胞疗法创新方向,根本在于其强大的基础科研转化能力、灵活的监管政策以及成熟的资本环境形成的协同效应。这三重力量相互赋能,共同构筑了美国细胞疗法长盛不衰的创新生态。
郑重声明:本文版权归原作者所有,转载文章仅为传播更多信息之目的,如作者信息标记有错误,请第一时间联系我们修改或删除,多谢。



Leave a Reply