干细胞外泌体这项新兴技术,正在经历从实验室走向临床的关键阶段。它不再只是科研论文里的概念,而逐渐成为多种疾病治疗的现实探索。过去几年中,全球已有超过 200 项相关临床试验启动,10 余个项目获批进入临床应用,这些数据让外泌体疗法从“潜力”变得更接近“证据”。
本文将从神经、代谢、骨科等重点疾病领域出发,结合近年的研究成果与实际案例,一起看看干细胞外泌体的真实治疗效果如何,以及它未来可能带来的医学新方向。

干细胞外泌体治疗效果揭秘:2025最新临床应用与研究进展
一、干细胞外泌体为何能“治病”?核心机制简述
干细胞外泌体的作用不是靠替代细胞去“长出新组织”,而是通过传递信号分子来改变受体细胞的行为,主要机制包括:
-
携带调控分子:蛋白质、mRNA、miRNA 等可调节细胞增殖、分化、凋亡和炎症反应。
-
免疫调节:能够抑制过度炎症、促进免疫耐受,适用于炎症性或免疫介导的损伤。
-
促进血管生成与基质重塑:有利于组织再生与上皮化过程。
通俗说:外泌体像“微型快递包裹”,把调节修复的指令送到受损组织,而不是直接变成新细胞。
二、干细胞外泌体治疗效果:8大主要疾病领域的临床应用进展
2025年8月6日,我国多家三甲医院在国际期刊《DovepressTaylor & Francis Group》上发表了一篇名为《干细胞来源的外泌体:生物医学应用、挑战和未来方向的综合回顾》的综述成果。[1]
综述全面介绍了干细胞外泌体(SC-Exos)在各个治疗领域的生物医学工程的临床应用,涵盖组织工程、先进的药物输送系统、心血管、神经系统、肿瘤、免疫、炎症、生殖、肌肉骨骼和皮肤病的治疗以及其他新兴应用。

干细胞来源的外泌体:生物医学应用、挑战和未来方向的综合回顾
1.心血管疾病中的应用
SC-Exos在心血管疾病中具有显著治疗潜力,适用于心肌梗死、缺血再灌注损伤、心脏重塑、纤维化及术后康复。其主要作用机制包括抗凋亡、抗炎、抗纤维化、促进血管生成,以及调节心肌细胞信号和代谢状态。(图1)
-
iPSC衍生内皮/心肌细胞外泌体:通过miR-100-5p或调控自噬信号(抑制mTOR、促进自噬通量)维持钙稳态,改善能量代谢,减少心肌细胞凋亡和纤维化,提高心肌存活率及左心室功能,动物实验显示显著缩小梗死面积并改善心室重塑。
-
BMSC-Exos:携带miR-143-3p抑制过度自噬和凋亡;靶向递送系统(CMP修饰的miR302-Exos)可促进心肌增殖、抑制炎症并激活Hippo/YAP信号,有效改善I/R损伤。
-
hUMSC-Exos工程化改造:IFN-γ激活或基因修饰可通过miRNA调控促进血管生成、抗凋亡和抗炎,显著改善心肌纤维化和心功能。
-
先进材料整合:可注射光固化水凝胶结合iPSC外泌体可提高稳定性、延长作用时间,并减少术后心包粘连风险。
总体来看,这些研究展示了SC-Exos在心血管治疗中的方法学多样性,包括miRNA货物装载、肽介导靶向递送及与生物材料整合的精准工程化策略,为心血管疾病提供安全、高效且可临床转化的无细胞治疗平台。
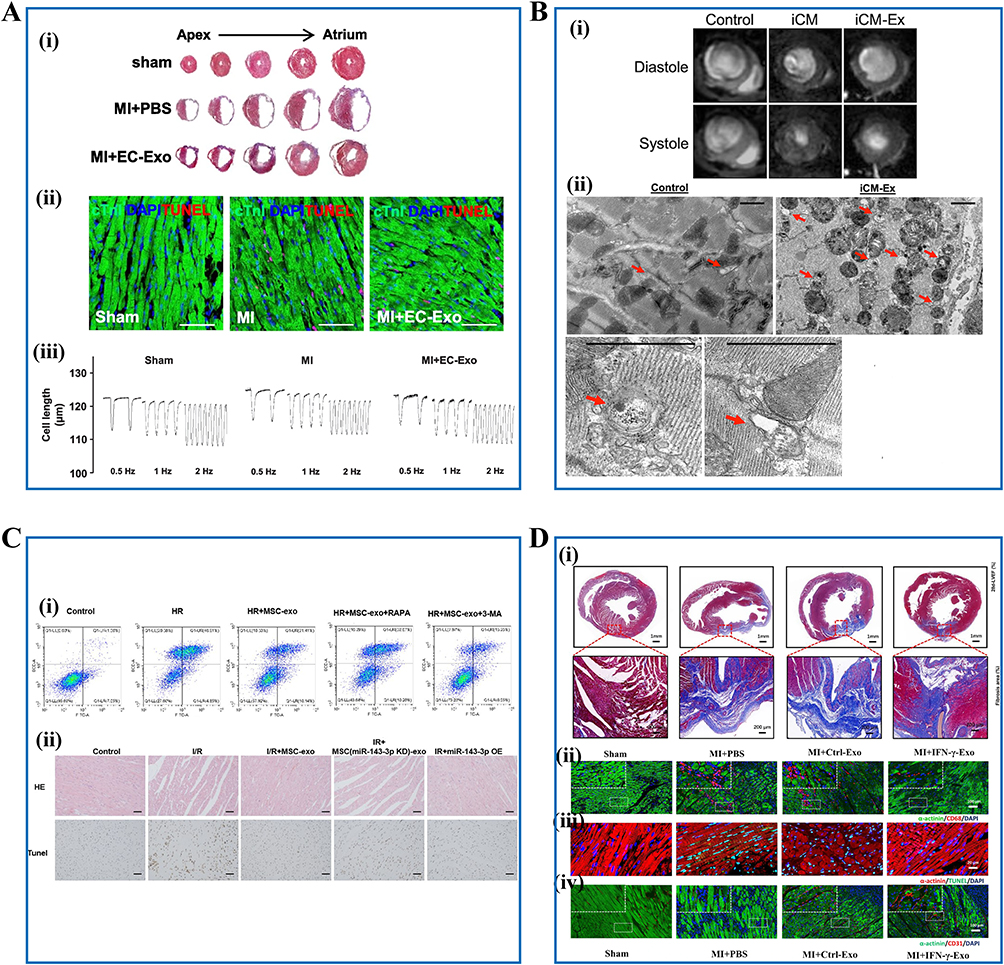
图1:干细胞外泌体在心血管疾病中的治疗应用
2.在神经系统疾病中的应用
SC-Exos在神经系统疾病中展现出多重治疗潜力,包括减少炎症、促进神经再生、改善线粒体功能及保护血脑屏障。其应用涵盖中风、脑外伤(TBI)、脊髓损伤(SCI)、阿尔茨海默病(AD)及药物成瘾等。(图2)
-
中风与脑缺血:MSC-Exos可通过miRNA调控改善神经功能。例如,Spion修饰的hUMSC-Exos增强血脑屏障穿透,将miR-1228-5p递送至TRAF6,改善线粒体功能、氧化应激和认知缺陷;ADSC-Exos抑制小胶质细胞铁死亡,改善炎症微环境;BMSC-Exos高表达miR-132-3p,可保护内皮细胞、减少氧化应激和凋亡,维持血管完整性。
-
脑外伤(TBI):SC-Exos与透明质酸胶原水凝胶结合可提供持续神经微环境,促进神经干细胞分化、血管化和脑结构重塑;hUMSC-Exos激活线粒体自噬,减少凋亡、焦亡和铁死亡,改善神经功能并减轻脑水肿。
-
脊髓损伤(SCI):基因改造的hUMSC-Exos通过miR-501-5p/肌球蛋白轻链激酶轴靶向新生血管内皮细胞,稳定血脊髓屏障、促进血管生成和轴突再生;与纤维蛋白胶结合可优化损伤微环境,促进神经修复、功能恢复及泌尿保护。
-
神经退行性疾病与药物成瘾:hUMSC-Exos通过miR-223调控PTEN-PI3K/AKT信号抑制AD细胞凋亡;BMSC-Exos可增强神经发生、抑制炎症,改善甲基苯丙胺成瘾小鼠的认知和空间记忆。
总的来说,SC-Exos通过多种分子机制为神经系统疾病提供安全、高效的神经保护和修复策略,展示了广阔的临床应用前景。

图2:干细胞外泌体在神经系统疾病中的治疗应用
3.癌症治疗中的应用
SC-Exos在癌症治疗中展现出巨大潜力,具有低免疫原性、高靶向性和良好的生物屏障穿透能力,可用于药物递送、基因调控和肿瘤微环境调节。(图3)
-
基因调控:BMSC-Exos通过递送特定miRNA抑制肿瘤信号通路,例如miR-30b-5p抑制PI3K/AKT,阻止非小细胞肺癌增殖和侵袭;miR-29b抑制胃癌腹膜转移。
-
药物递送:外泌体可负载化疗药物(如阿霉素、紫杉醇),结合靶向修饰(如粘蛋白1适体、SDF1-CXCR4轴、环肽cRGDyK)实现高效靶向递送,提高抗肿瘤活性并降低全身毒性,例如结直肠癌、骨肉瘤及胶质母细胞瘤。
-
肿瘤微环境调控:BMSC-Exos可影响乳腺癌化疗耐药机制,如miR-21-5p增强耐药性,而抑制该miRNA可逆转耐药;装载miR-3182的hUMSC-Exos可抑制三阴性乳腺癌增殖、迁移和侵袭,并诱导凋亡。
总的来看,SC-Exos在癌症治疗中兼具基因调控、药物递送和微环境调节功能,为精准外泌体疗法提供理论基础。但仍需优化外泌体的装载效率、靶向性及临床安全性,以推动临床转化。
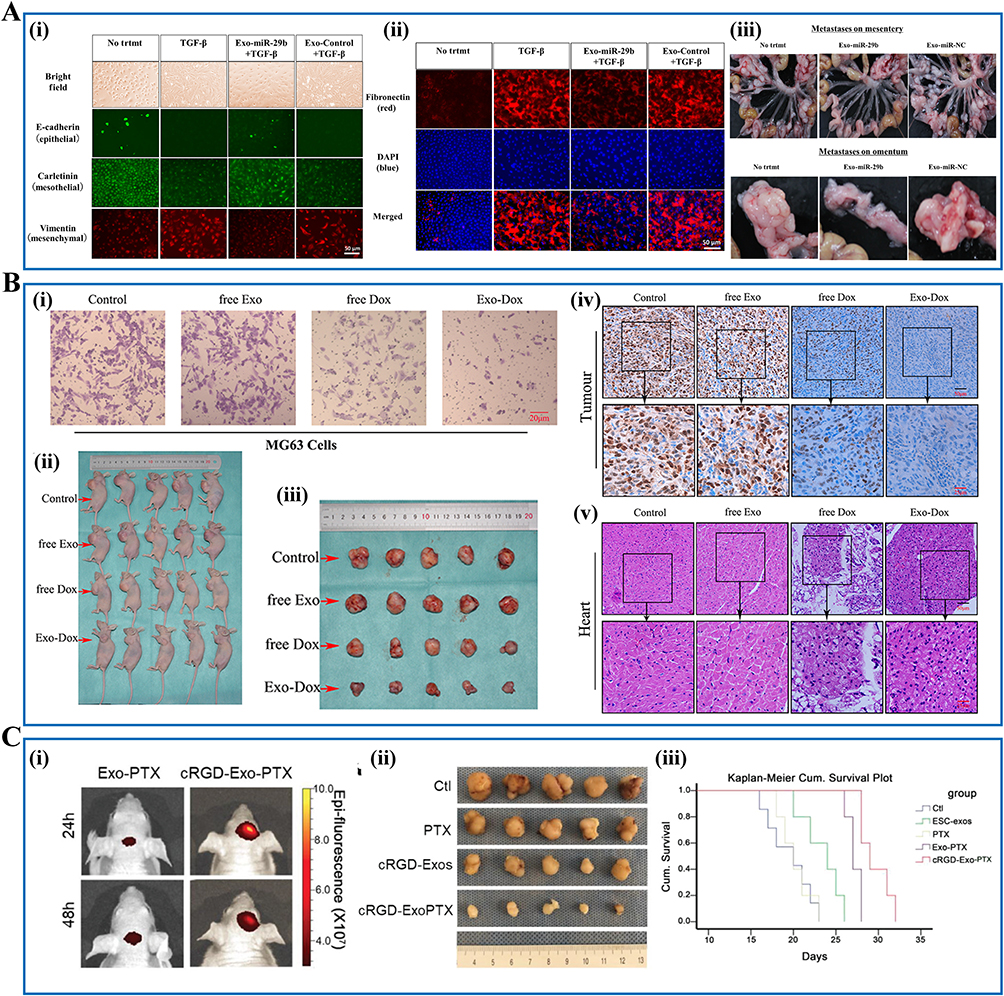
图3:干细胞外泌体在癌症治疗中的应用
4.在免疫调节和炎症相关疾病中的应用
SC-Exos在炎症性肠病(IBD)、全身炎症、自身免疫性疾病和急性移植物抗宿主病(aGVHD)等免疫相关疾病中展现出显著疗效。(图4)
-
IBD:富含miR-129-5p的hUMSC-Exos可靶向铁死亡通路,减少脂质过氧化和炎症,促进肠道屏障修复与上皮再生;通过miR-146a/SUMO1轴调控可延缓结肠炎相关癌症进展。
-
全身炎症与脓毒症:IL-1β预处理的BMSC-Exos激活Sirt1/ERK通路,增强内质网应激调节,减轻肺损伤和全身炎症;miR-27b可抑制NF-κB信号,降低促炎因子并改善多器官功能障碍。
-
自身免疫性疾病:BMSC-Exos通过miR-16/miR-21调控巨噬细胞极化,减轻SLE炎症和肾损伤;丝蛋白水凝胶包裹的嗅粘膜MSC-Exos可抑制T滤泡辅助细胞极化,促进Treg生成,改善类风湿性关节炎炎症与关节损伤。
-
aGVHD:BMSC-Exos调节树突状细胞和T细胞亚群,降低促炎因子并增加Treg比例,缓解症状并提高存活率;牙龈MSC-Exos可抑制M1巨噬细胞炎症反应,提升IL-10水平,改善高脂环境下的炎症状态。
总体而言,SC-Exos通过多种miRNA和信号通路调控免疫反应,显示出广泛的抗炎和免疫调节潜力,为免疫相关疾病的精准治疗提供了有力策略。
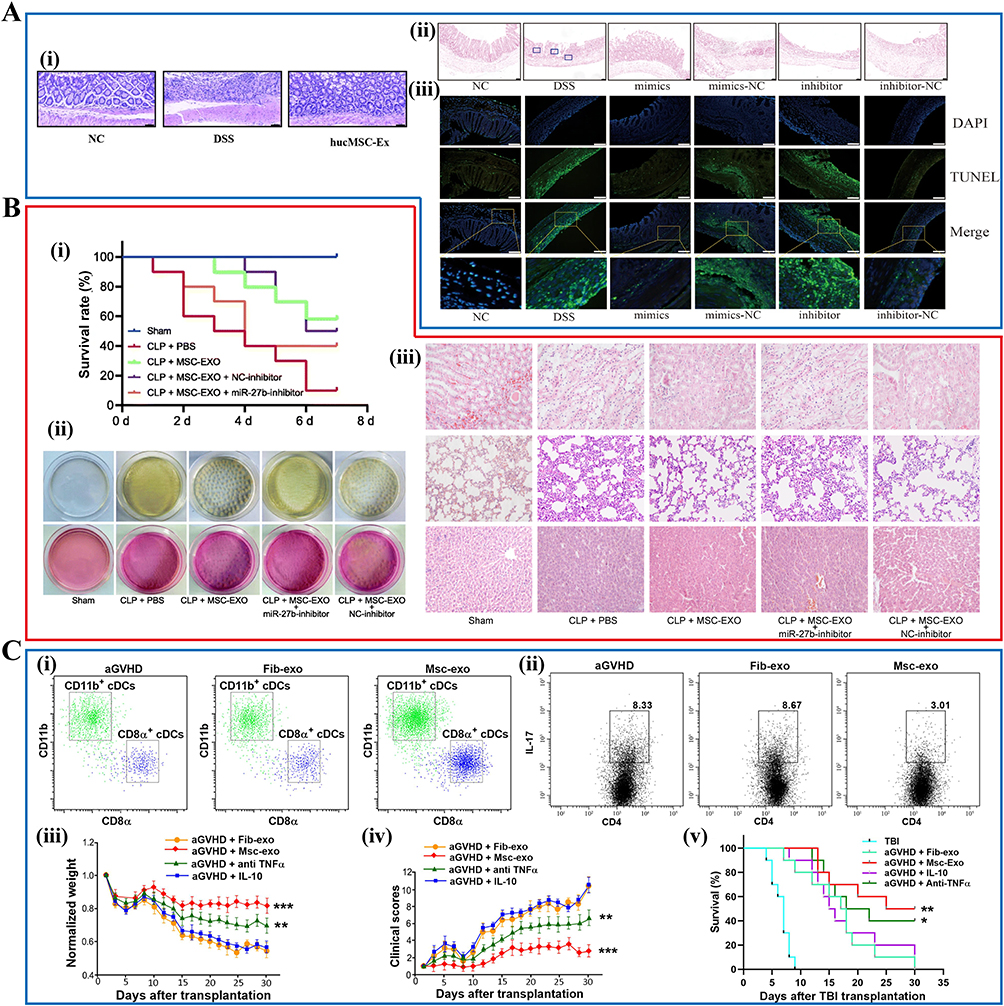
图4:干细胞外泌体在免疫调节和炎症相关疾病中的治疗应用
5.生殖系统和生育保护中的应用
SC-Exos在男性和女性生殖系统疾病及生育力保存方面展现出广泛潜力。与传统激素替代疗法或侵入性操作相比,SC-Exos可非侵入性给药、副作用低,并具靶向治疗效果,无全细胞移植相关风险。(图5)
-
女性生殖系统:SC-Exos通过调节炎症、氧化应激、细胞凋亡和纤维化,促进卵巢功能恢复和子宫内膜再生。BMSC-Exos可通过miR-144-5p/PTEN下调抑制颗粒细胞凋亡,改善化疗导致的卵巢衰竭;hUMSC-Exos递送miR-145-5p抑制XBP1,减轻氧化损伤;负载miR-21-5p的BMSC-Exos可调控Notch信号改善卵巢结构和激素合成;在子宫内膜修复中,hUMSC-Exos通过miR-140-3p/FOXP1/Smad及Hippo通路减轻纤维化,改善生殖能力。
-
男性生殖系统:SC-Exos在睾丸衰老、化疗损伤和精子发生恢复中表现出疗效。hUMSC-Exos通过调节巨噬细胞极化、减少氧化应激,促进睾丸细胞增殖、精原干细胞微环境恢复和睾酮合成,改善精子生成;在勃起功能障碍中,多次注射BMSC-Exos可增强海绵体压力、增加平滑肌含量、激活NO/cGMP信号并促进血管生成与细胞增殖,从而改善功能。
总体而言,SC-Exos通过多种分子机制为生殖系统疾病提供安全、有效且精准的治疗和生育力保护策略。
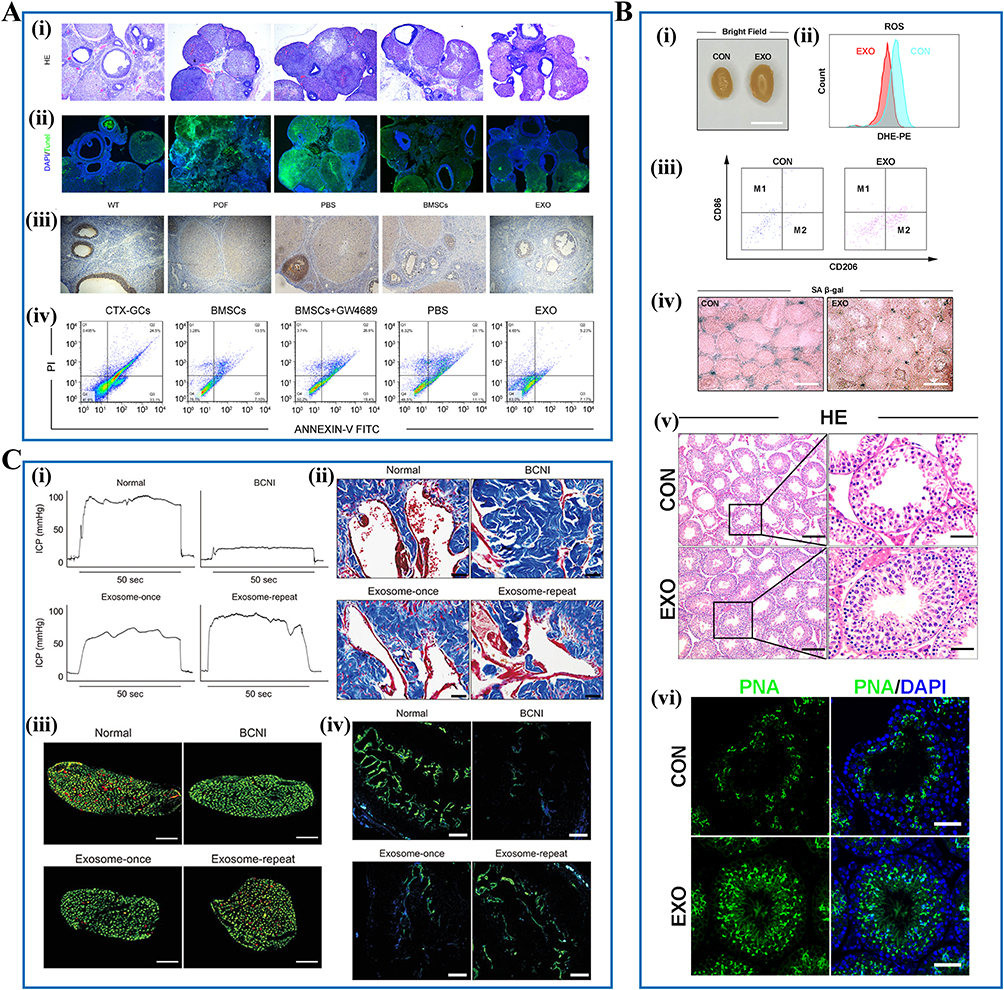
图5:干细胞外泌体在生殖系统和生育保护中的应用
6.在骨和软骨组织修复中的应用
SC-Exos因其出色的生物学特性,在骨和软骨组织修复中展现出显著潜力。它们通过递送特定核酸、蛋白质和脂质,调节细胞行为、促进组织再生并优化免疫微环境,为传统治疗局限性提供新解决方案。(图6)
-
骨组织修复:SC-Exos可增强成骨能力。例如,将成骨诱导的BMSC-Exos与GelMA水凝胶结合,可持续释放外泌体,促进BMSC成骨分化和血管生成;hUMSC-Exos/Gel/nHP复合支架通过miR-21调控VEGF-A和HIF-1α、抑制NOTCH1/DLL4通路,加速颅骨缺损修复;BMSC-Exos通过miRNA调控BMP2和ACVR2B,激活Smad1/5/9信号,进一步增强骨再生能力。
-
软骨修复:hUMSC CD56+外泌体结合脱细胞基质水凝胶可缓释作用,促进半月板愈合,保护关节软骨并抑制退变;锂掺杂生物玻璃陶瓷通过提升BMSC-Exos中miR-455-3p水平,增强软骨细胞增殖、迁移和基质合成,有效促进软骨再生。
-
骨-软骨界面修复:MMP1敏感自组装肽水凝胶(KGE)可时空控制释放BMSC-Exos,募集CD90+干细胞,促进骨血管形成及骨修复,同时增强干细胞迁移和极化能力,为复杂骨-软骨损伤提供创新治疗方案。
总体而言,SC-Exos在骨、软骨及骨-软骨界面修复中具有多维调控能力,展示了广阔的临床应用前景。
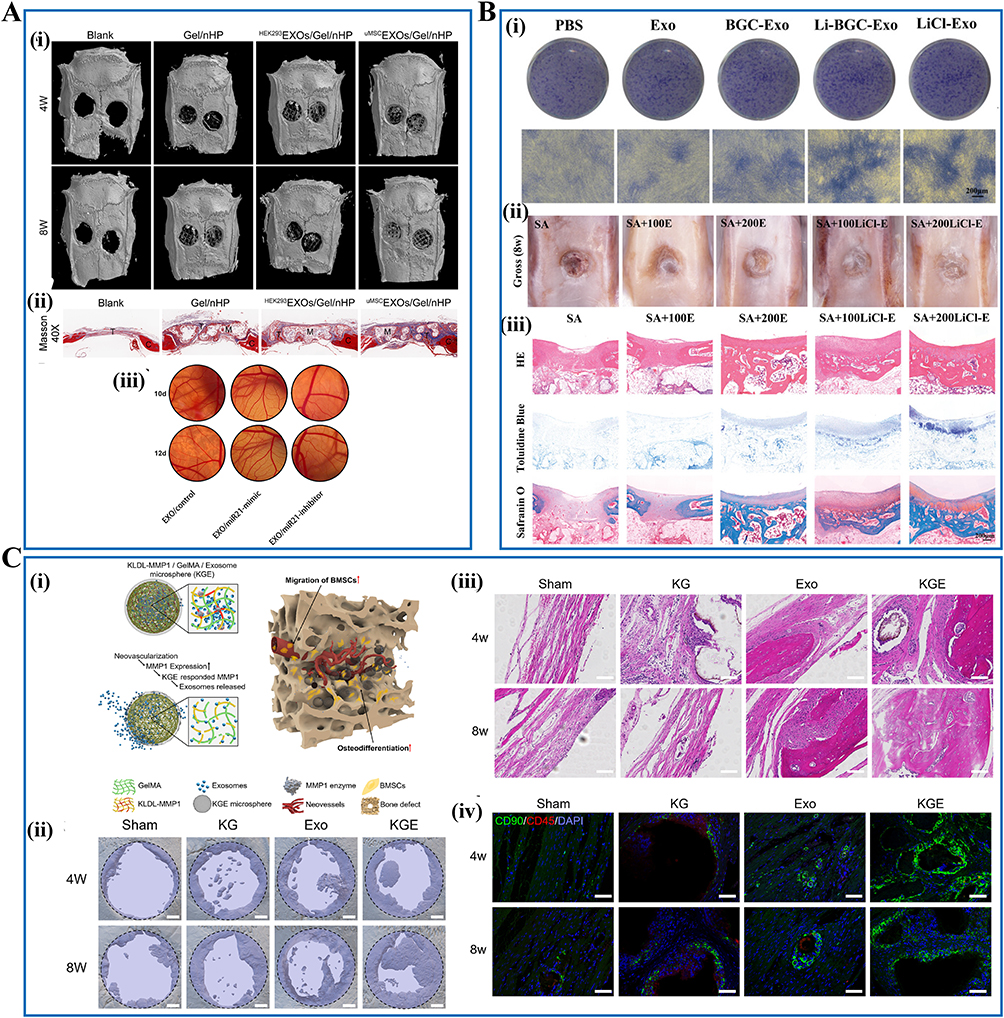
图6:干细胞外泌体在骨和软骨组织修复中的治疗应用
7.在皮肤伤口愈合和组织修复中的应用
SC-Exos因其出色的生物学特性,在皮肤伤口愈合和组织再生中展现出巨大潜力。它们通过促进细胞迁移和增殖、调节炎症、加速血管生成及增强细胞外基质重塑,有效加快伤口愈合。(图7)
-
糖尿病慢性伤口:3D培养的ADSC-Exos结合多功能水凝胶可持续释放外泌体,增强血管生成、胶原沉积和巨噬细胞极化,显著促进愈合。温敏性PF-127水凝胶和明胶银纳米粒子微针载体进一步延长外泌体滞留时间,提高抗菌和再生效果。
-
烧伤治疗:iPSC衍生角质形成细胞外泌体通过miR-762促进角质形成细胞和内皮细胞迁移,加速血管生成和上皮再生;磁性Fe3O4标记的hUMSC-Exos在外部磁场引导下增强靶向迁移,加快伤口愈合并减少疤痕形成。
-
瘢痕与纤维化控制:MSC-Exos可通过抑制TNF超家族/NF-κB通路,调节成纤维细胞增殖和迁移,减少纤维化和增生性瘢痕。
-
抗氧化与皮肤保护:hUMSC-Exos通过调控Nrf2防御系统、减少ROS生成、改善线粒体功能和钙信号,修复氧化应激损伤,对紫外线及其他氧化应激相关皮肤损伤具有显著效果。
总体而言,SC-Exos通过多种机制显著改善皮肤伤口愈合、组织再生和抗氧化能力,展示了广阔的临床应用前景。
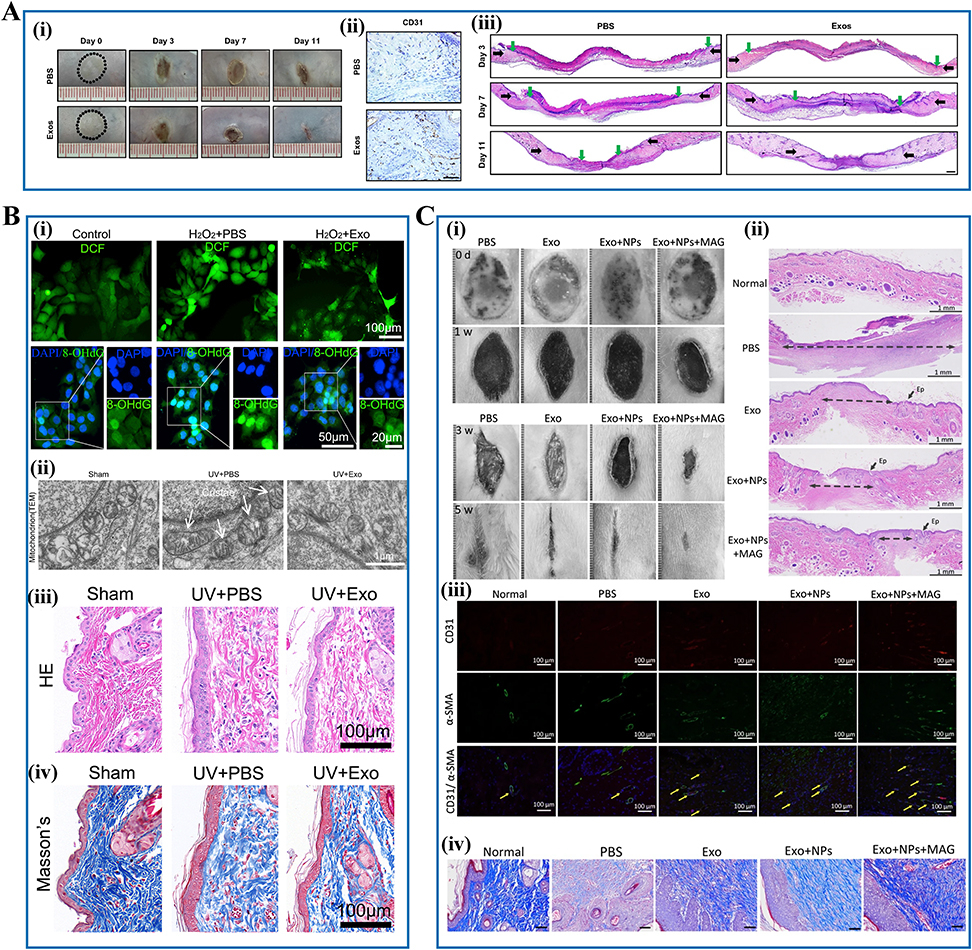
图7:干细胞外泌体在皮肤伤口愈合和组织修复中的治疗应用
8.在其他疾病治疗中的应用
除了心血管、神经退行性疾病和癌症,SC-Exos在视网膜疾病、肝纤维化、急性肾损伤(AKI)、口腔组织再生、脂肪移植存活、肺纤维化和角膜修复等多种疾病中也展现出显著潜力。它们通过递送特定miRNA或蛋白质,调节细胞凋亡、炎症和免疫微环境,促进组织修复和功能恢复。(图8)
-
视网膜疾病:hUMSC-Exos递送miR-22-3p抑制MAPK通路,保护视网膜神经节细胞,改善视网膜结构和功能。
-
肝纤维化:hUMSC-Exos携带miR-148a调控STAT3通路,促进巨噬细胞由M1向M2极化,减轻纤维化。
-
急性肾损伤(AKI):BMSC-Exos修复近端小管上皮细胞极性、屏障完整性并促进细胞增殖,有效缓解缺氧损伤。
-
口腔组织再生:牙髓干细胞Exos通过抑制IL-6/JAK2/STAT3通路及M1→M2极化,促进牙槽骨和牙周组织修复。
-
脂肪移植:ADSC-Exos结合PF-127水凝胶激活HIF-1α/VEGF信号,提高移植脂肪存活率。
-
肺纤维化:BMSC-Exos富含miR-466f-3p,抑制c-MET/AKT/GSK3β通路,逆转肺泡上皮间质转化,减轻放射性肺损伤。
-
角膜修复:iMSC-Exos结合温敏性壳聚糖水凝胶递送miR-432-5p,减少胶原过度沉积,促进上皮与基质修复,降低瘢痕形成。
此外,外泌体标记和追踪技术(如NIR-II荧光Pdots-Glu)可实现体内长期追踪,精确监测和优化治疗效果,为临床转化提供支持。
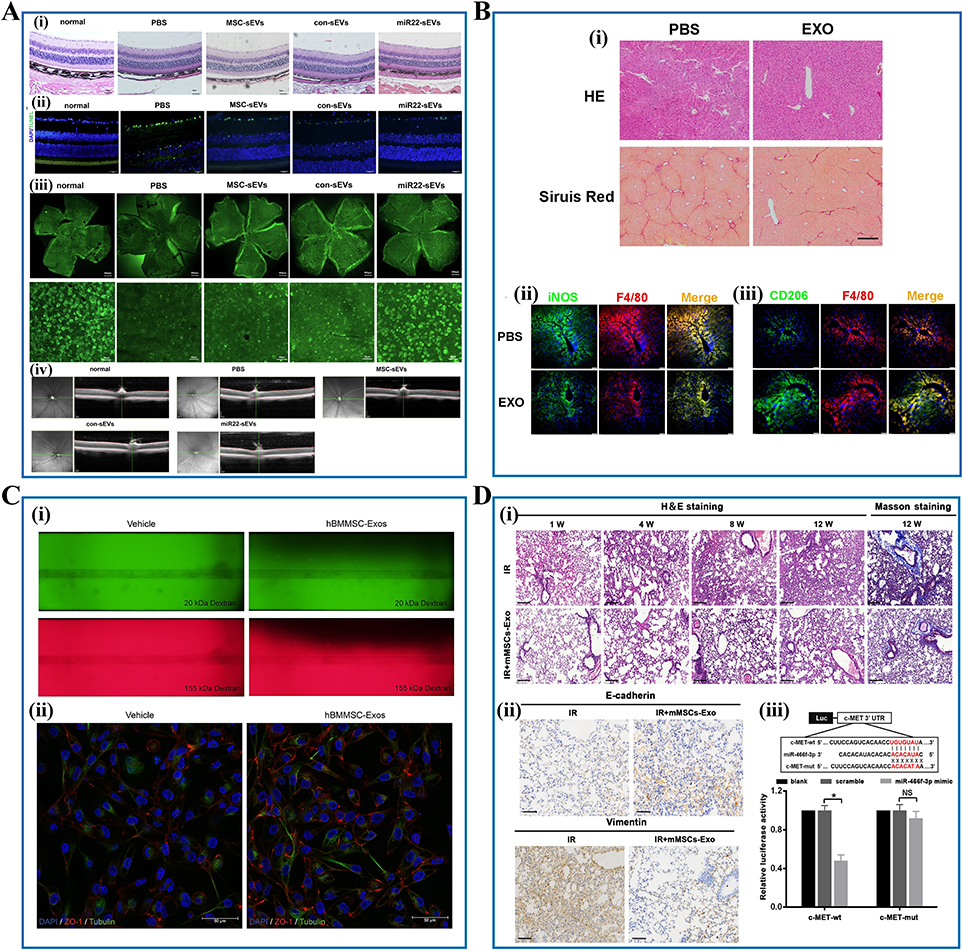
图8:干细胞外泌体在其他疾病治疗中的治疗应用
三、干细胞外泌体的临床转化现状
干细胞外泌体(SC-Exos)在临床研究中显示出广泛的治疗潜力和良好安全性,涉及皮肤疾病、伤口愈合、IBD、脊髓损伤(SCI)、COVID-19肺炎等多个领域。早期I/II期临床试验表明,多来源的SC-Exos(如hUMSC-Exos、ADSC-Exos、AMSC-Exos等)可通过多种给药方式(注射、局部、雾化、微针等)实现组织修复、免疫调节和器官功能改善,且不良事件轻微、可逆。显著疗效包括瘘管闭合率提升、神经功能改善、皮肤质量提升、毛发密度增加以及干眼症状缓解。
然而,现有证据存在局限:样本量小(5–30人)、随访时间短(多为3–6个月)、外泌体来源、制备、给药方式和剂量差异大,导致研究异质性高。这凸显了建立标准化生产工艺、统一给药方案和更大规模验证性试验的迫切需求。
在监管方面,SC-Exos在不同国家面临不同分类和审批要求。例如,美国FDA将其归类为生物药品,需遵循cGMP标准并提交全面的临床前和临床数据。其异质性和作用机制复杂,增加了质量控制和批次一致性管理难度。当前FDA批准产品有限,市场上仍存在大量监管不合规现象(约68%企业未明确监管状态),显示出对清晰监管指导的迫切需求。
总的来看,SC-Exos在临床应用中安全性良好、疗效潜力大,但临床转化仍受限于标准化生产、监管复杂性和验证性试验不足,需要系统化规范和国际协调以加速其临床落地。
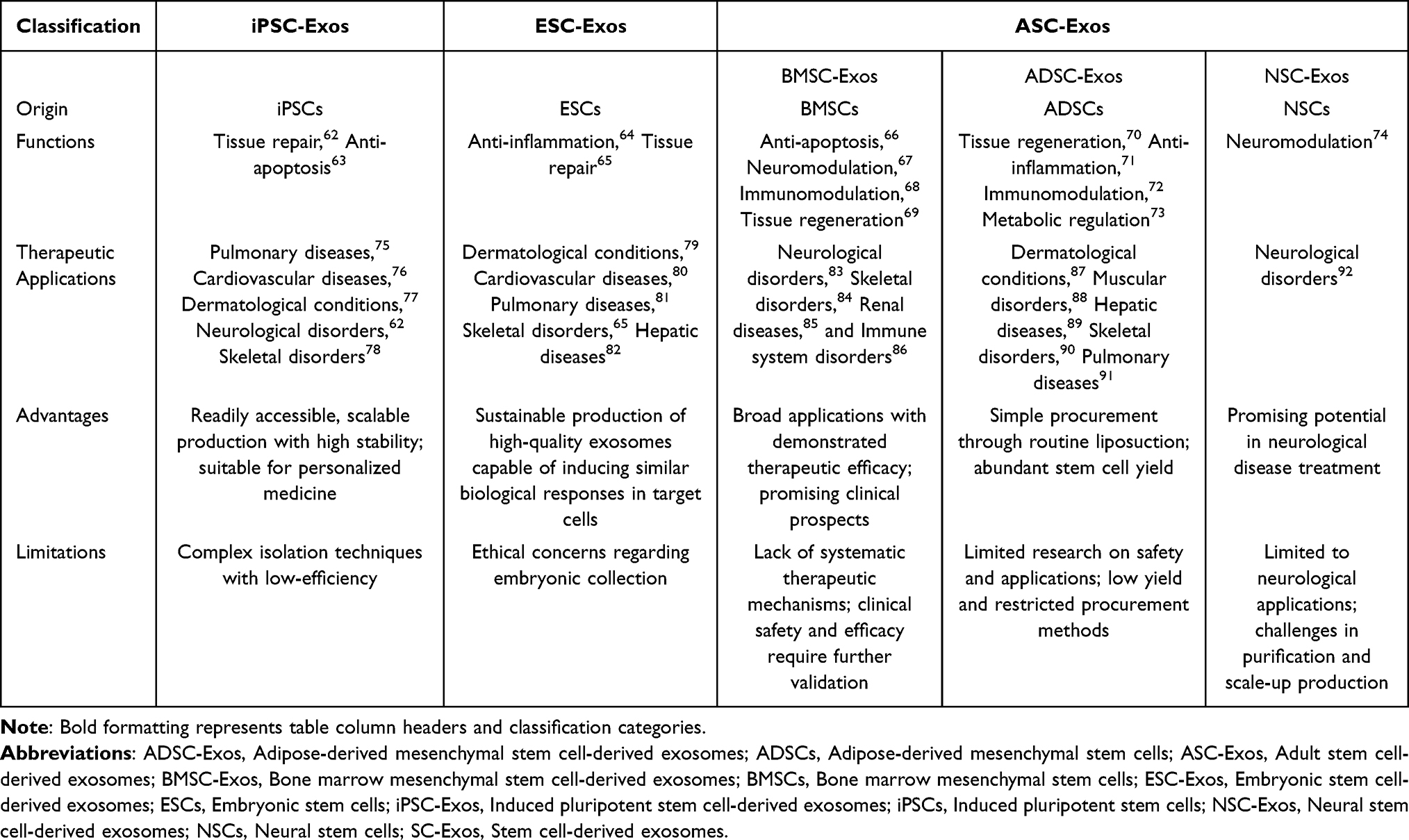
干细胞外泌体全球临床试验汇总
四、临床应用面临的挑战
尽管SC-Exos在多种疾病中显示出广泛的治疗潜力,但其临床转化仍存在不少问题。
制备与质量控制:目前缺乏统一标准,不同实验室采用的分离方法(如超速离心、SEC)差异大,导致产物纯度和疗效不稳定。常用标志物(CD63、CD81)无法全面反映功能,分析技术(电子显微镜、纳米颗粒追踪、流式细胞术)存在污染、重复性差和效率低的问题。缺乏对功能分子和生物活性的统一评价标准,也让研究结果难以直接比较。
治疗异质性:SC-Exos组成受干细胞类型、供体差异和培养条件影响大。不同来源或处理方式的外泌体对同一疾病的疗效可能差异显著。体外扩增、长期培养或多次传代会影响外泌体特性,而系统研究对此仍有限。
规模化生产:大规模制备需要严格无菌条件和稳定活性,尽管有基因工程、3D培养等技术提高产量,但可能改变外泌体功能,实际效果难以预测。
给药途径与剂量:不同给药方式(静脉、局部、鼻腔)和剂量会显著影响体内分布和疗效。例如,鼻腔给药在某些神经疾病中比静脉注射更靶向、更非侵入性,但缺乏系统比较研究。剂量差异也让疗效比较困难。
生物安全性:虽然SC-Exos总体安全性高,但在癌症治疗中可能有双重作用,既可能抑制,也可能促进肿瘤生长。长期重复给药的安全性和免疫原性数据仍有限,尤其是生殖系统应用,需要特别关注脱靶效应和生育影响。
总结:SC-Exos潜力巨大,但临床转化仍需解决标准化制备、异质性控制、规模化生产、给药优化和安全性评估等问题。未来需要多中心、大规模、长期随访的标准化临床研究,确保其在临床中安全有效应用。
总结与展望
干细胞外泌体(SC-Exos)正从实验室研究走向临床实践,正在成为多种疾病治疗的真实探索工具。它通过递送蛋白质、miRNA等分子信号调控受损组织的行为,而不是直接替代细胞,展现出免疫调节、抗炎、促进再生和血管生成等多重作用。近年来,无论在心血管、神经系统、癌症、免疫疾病,还是在生殖、骨软骨和皮肤修复等领域,SC-Exos都显示了令人期待的治疗效果,并在临床试验中初步证明了安全性和可行性。
然而,临床应用仍面临一些挑战:制备和质量控制缺乏统一标准,外泌体来源和培养条件差异大导致疗效不稳定;大规模生产和功能保持存在技术难题;不同给药途径、剂量和长期安全性仍需系统研究;在癌症及生殖系统应用中尤其需要关注潜在风险。
总体来看,SC-Exos拥有广阔的临床前景和创新潜力,但要真正走向广泛应用,还需要标准化生产、功能评价体系、给药优化及长期随访的多中心临床研究。随着技术不断突破和研究深入,干细胞外泌体有望成为无细胞治疗领域的核心工具,为复杂疾病提供全。
参考资料:
[1]Zhang J, Tian X, Li Y, Fang C, Yang F, Dong L, Shen Y, Pu S, Li J, Chang D, Lei L, Yu X. Stem Cell-Derived Exosomes: A Comprehensive Review of Biomedical Applications, Challenges, and Future Directions. Int J Nanomedicine. 2025;20:10857-10905
https://doi.org/10.2147/IJN.S527137免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。
郑重声明:本文版权归原作者所有,转载文章仅为传播更多信息之目的,如作者信息标记有误,请第一时间联系我们修改或删除,多谢。


发表回复