摘要:帕金森病(PD)的干细胞替代疗法虽前景广阔,但移植后多巴胺能(DA)神经元极低的存活率(>90%的丢失)严重阻碍其疗效。本文聚焦于这一核心挑战,综述了近期突破性研究揭示的细胞死亡关键机制——TNFα-NFκB-p53信号轴,并提出了两项核心解决方案:
- 1)短期使用临床批准的TNFα抑制剂(如阿达木单抗) 以阻断该死亡通路;
- 2)利用特定细胞表面标志物(CD49e^low/CD184^high)进行无基因工程化的DA神经元纯化,以消除非目标细胞带来的风险。
这两大策略相辅相成,为提升移植细胞存活率、推动PD细胞疗法走向安全有效的临床转化提供了明确路径。
干细胞治疗帕金森病:提高人干细胞源多巴胺能神经元存活率的两种方法
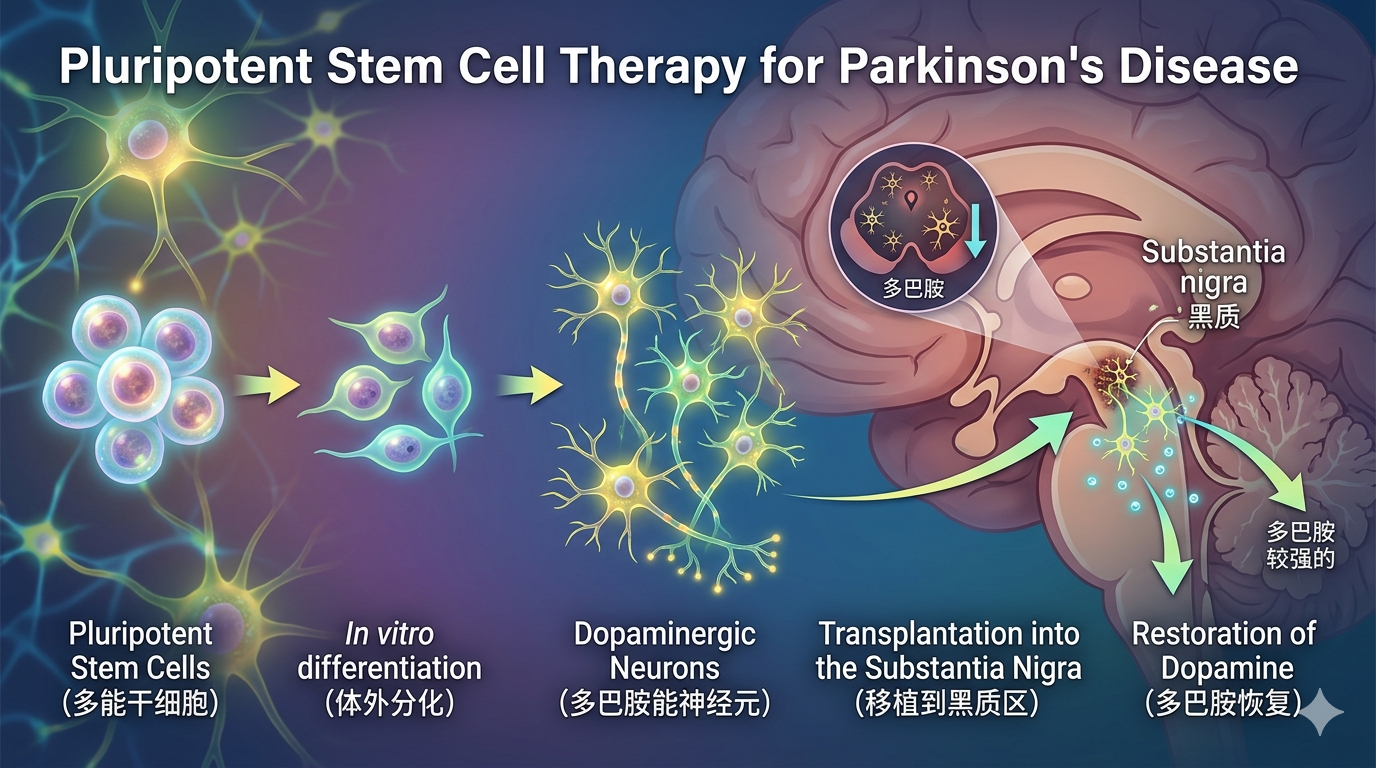
帕金森病(PD)作为第二常见的神经退行性疾病,其核心病理特征是中脑黑质多巴胺(DA)能神经元的进行性退化,导致运动功能严重受损。现有药物如左旋多巴仅能对症治疗,无法逆转疾病进程。基于人多能干细胞(hPSC,包括胚胎干细胞和诱导多能干细胞)的细胞替代疗法,旨在通过移植新的DA神经元从根本上恢复神经环路功能,被视为极具前景的治愈性策略,并已进入临床试验阶段。
然而,该疗法的转化面临严峻挑战。其中最突出的是移植后DA神经元的存活率极低,超过90%的细胞在移植后死亡,导致疗效不稳定且不可预测。同时,移植产物中混杂的非DA细胞(如血清素能神经元)可能引发移植物诱导的运动障碍等副作用。因此,如何提高移植DA神经元的存活率并确保产物纯度,成为领域内亟待解决的核心科学问题。

核心挑战剖析:移植神经元为何大量死亡?
近期研究为揭示细胞死亡机制带来了突破。Kim等人(2024)利用体内CRISPR-Cas9筛选技术发现,肿瘤抑制蛋白p53是限制移植后DA神经元存活的关键因子(图1)。这一发现与PD病理中p53水平升高的现象相吻合。进一步研究发现,在移植早期,肿瘤坏死因子-α(TNFα) 通过激活核因子κB(NFκB)信号,进而上调并激活p53,最终启动DA神经元的程序性死亡。值得注意的是,这种TNFα不仅来源于宿主免疫反应,移植的DA神经元自身也会表达TNFα,形成一种自我限制的“细胞自主性死亡”环路。
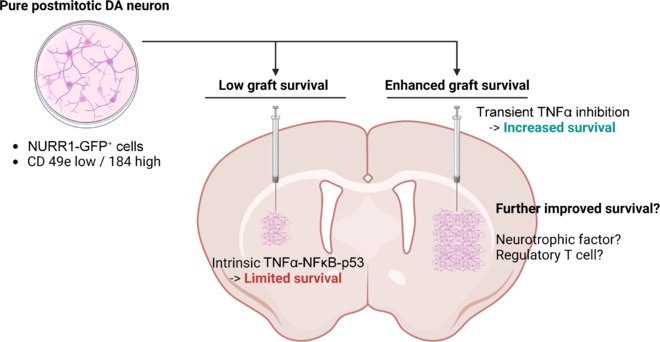
解决方案一:靶向死亡通路——短暂抑制TNFα信号
既然TNFα-NFκB-p53轴是导致死亡的关键通路,抑制该通路就成为提高存活率的直接策略。研究表明,在移植后关键窗口期,短期使用临床已广泛应用的TNFα抑制剂(如阿达木单抗),能显著提高临床前动物模型中移植DA神经元的存活率,并伴随运动功能的改善。
此策略的优势在于:
- 1)转化速度快:阿达木单抗等药物安全性已知,“老药新用”可大幅缩短研发周期;
- 2)治疗窗口明确:仅在移植前后短期给药,即可有效阻断早期死亡潮,避免长期免疫抑制的潜在风险。
解决方案二:优化移植细胞产品——无基因标记的DA神经元纯化
提高存活率不仅需要“救活”细胞,还需从源头优化移植细胞本身。传统依赖遗传报告基因(如NURR1-GFP)的纯化方法因涉及基因工程而不适于临床。为解决此问题,研究者通过筛选鉴定出一组细胞表面标志物组合:CD49e (低表达) 和 CD184 (高表达)。利用流式细胞术分选该标志物阳性的细胞,即可在不进行基因改造的前提下,高效富集到高纯度的、有丝分裂后的DA神经元。
这一纯化策略的意义重大:
- 1)临床兼容性好:适用于任何hPSC/iPSC系,为自体或异体治疗提供了通用方案;
- 2)提升安全性与疗效:去除非目标细胞,降低了运动障碍等副作用风险,并可能富集对PD治疗至关重要的、易受损的A9亚型DA神经元;
- 3)保证产品一致性:为标准化细胞制剂生产奠定了基础。
临床转化前景与综合应用
将上述两大策略——围移植期短期TNFα抑制与移植前基于表面标志物的DA神经元纯化——相结合,构成了一个协同增强的解决方案。前者为移植细胞创造了初始生存窗口,后者则提供了最优化的“种子”细胞。
这一策略的价值不仅限于PD。TNFα介导的炎症性死亡是许多细胞移植面临的共性障碍,因此该方案为其他疾病的细胞治疗(如视网膜细胞治疗黄斑变性、胰岛细胞治疗糖尿病)提供了重要参考。此外,流行病学数据提示,长期使用TNFα抑制剂的患者PD发病率降低,暗示该策略可能对原生神经元也有保护作用,或有利于移植物的长期整合。
未来展望与待解问题
尽管前景光明,仍有诸多问题有待探索:
首先,TNFα抑制仅解决了约30%的细胞死亡,其余死亡机制(如移植过程中的缺氧应激)需要进一步阐明。
其次,需要优化TNFα抑制剂的最佳给药方案(时机、剂量、疗程)。
最后,探索将上述策略与神经营养因子输送、或与具有免疫调节功能的细胞(如调节性T细胞)共移植等联合方案,有望进一步优化移植微环境,实现存活率的阶梯式提升。
结论
综上所述,通过精准解析移植后DA神经元死亡的核心通路(TNFα-NFκB-p53轴),并据此开发出药理学干预与细胞产品工程化的双轨策略,我们为突破帕金森病干细胞疗法存活率低的瓶颈提供了清晰、可转化的路径。这些进展不仅推动了PD细胞治疗向临床现实迈进,也为整个细胞替代治疗领域树立了攻克移植存活难题的典范。
郑重声明:本文版权归原作者所有,转载文章仅为传播更多信息之目的,如作者信息标记有误,请第一时间联系我们修改或删除,多谢。



发表回复