2026年,神经退行性疾病(NDs)依然是医学界亟待攻克的堡垒。帕金森病(PD)、阿尔茨海默病(AD)、肌萎缩侧索硬化症(ALS)及亨廷顿病(HD)以进行性神经元丢失为核心,夺走了无数患者的生活质量。传统治疗多局限于对症治疗,难以实现神经修复。
干细胞疗法作为一种潜在的“范式革新”治疗策略,有望通过细胞替代、免疫调节和营造神经保护微环境,为NDs患者带来福音。近年来,干细胞治疗神经退行性疾病方面研究取得了显著进展,但也面临着免疫排斥、肿瘤风险、伦理争议等挑战。
干细胞疗法治疗神经退行性疾病:2026最新综述,解析AD、PD与ALS的修复密码
本期我们将深入解析《内科与外科年鉴》发表的题为“干细胞在神经退行性疾病治疗中的应用:进展、见解与挑战”的最新综述,为您全面复盘干细胞疗法的最新科研证据、治疗机制及临床转化面临的障碍。

该文系统评估了不同干细胞类型在治疗上述疾病中的潜力,聚焦其作用机制、递送路径及实验证据。结果表明,胚胎干细胞(ESCs)、间充质干细胞(MSCs)、诱导多能干细胞(iPSCs)及神经干细胞(NSCs)均展现出独特的再生特性;其中,MSCs衍生的外泌体因能穿透血脑屏障并延长神经元寿命而备受关注。当前研究涉及的给药途径包括静脉注射、鼻腔给药及直接脑移植。针对PD、AD、HD及ALS的治疗获益已获广泛验证。
干细胞治疗神经退行性疾病:2026最新综述,解析AD、PD与ALS的修复密码
一、方法论
我们的团队对“干细胞在神经退行性疾病中的治疗潜力:进展、见解和挑战”这一主题进行了全面检索。我们使用关键词“干细胞疗法”、“神经退行性疾病”、“阿尔茨海默病”、“帕金森病”和“干细胞移植”在PubMed数据库中检索了过去5年的相关文献。
纳入的文献类型包括荟萃分析、系统评价、综述研究、临床试验和随机对照试验。此外,我们还从Cochrane图书馆和ClinicalTrials.org网站检索了近一年内发表的临床试验。我们从Cochrane图书馆检索到1项试验;从ClinicalTrials.org网站检索到11项试验;从PubMed数据库检索到223项研究,并对这些研究进行了相关性筛选。最终,31项研究被纳入最终稿。
所有纳入研究均符合PICO标准:研究对象为PD、AD、ALS及中风等神经退行性疾病患者;干预措施涵盖MSCs、脂肪来源干细胞、骨髓干细胞、ESCs、骨骼肌干细胞、多能干细胞及人类胎儿腹侧中脑干细胞;对照设为不治疗或标准治疗;结局指标包括疾病进展延缓、生活质量改善、生存期延长及持续临床获益。
二、干细胞的分类和特征
干细胞疗法,又称再生疗法,旨在修复神经退行性疾病中受损的结构细胞,促进功能性细胞的有效补充。其核心目标在于补偿丢失细胞,或营造利于修复的微环境。干细胞具备自我更新、增殖及多向分化能力。本文聚焦以下四类:胚胎干细胞(ESCs)、诱导多能干细胞(iPSCs)、间充质干细胞(MSCs)及神经干细胞(NSCs)。图1(A)展示了多能干细胞的主要来源。
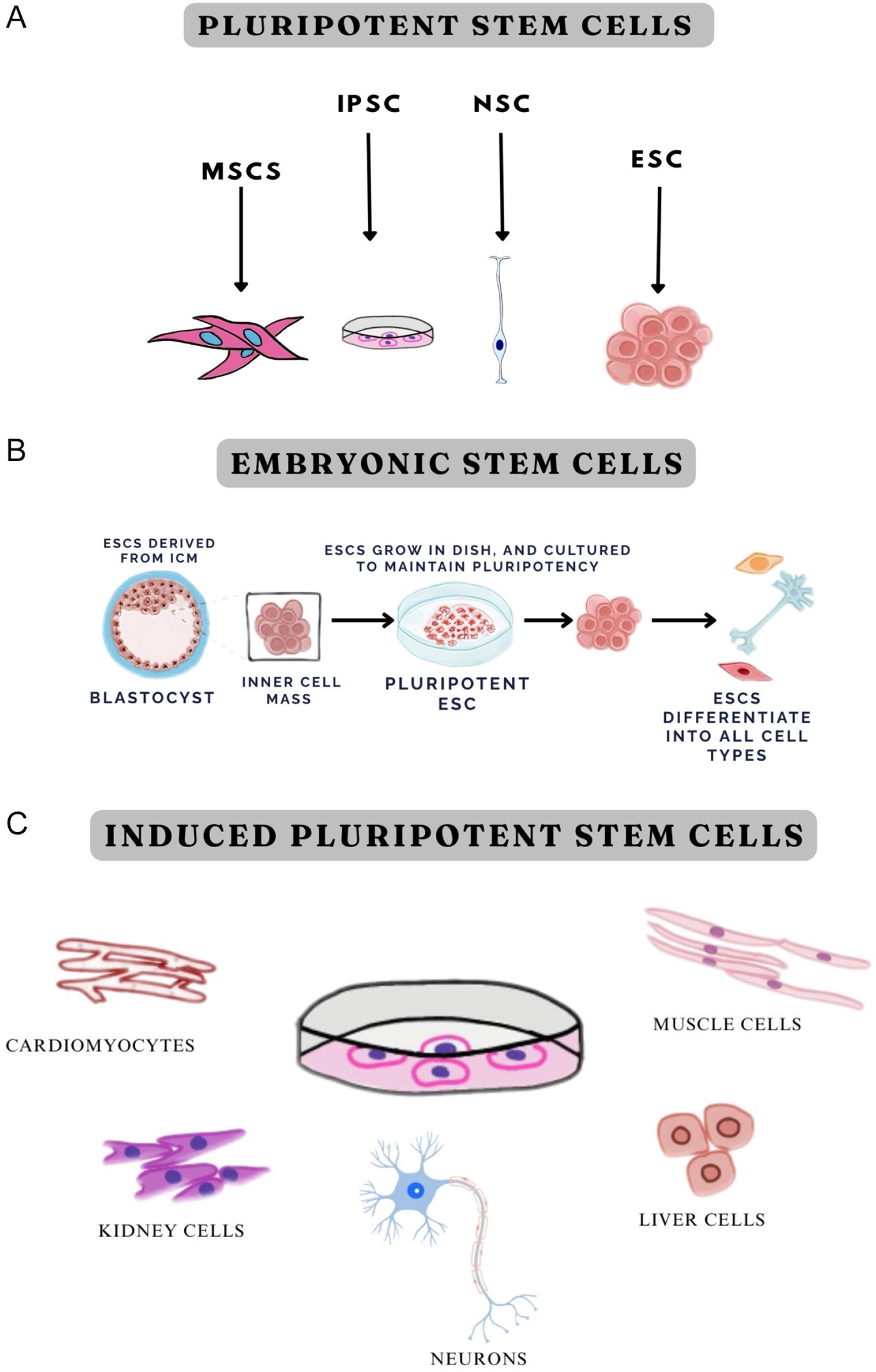
图1:多能干细胞的分类和来源。(A) 多能干细胞的来源。(B) 胚胎干细胞的来源和分化过程。(C) 诱导多能干细胞的来源。
胚胎干细胞:巨大的潜力与显著的争议
胚胎干细胞(ESCs)因其独特的“多能性”——即分化为体内任何细胞类型的能力——而被视为再生医学领域最具前景的细胞来源之一。尤其在帕金森病(PD)的研究中,ESCs能分化为产生多巴胺的神经细胞,已在动物模型中展现出良好的治疗效果。
然而,这种强大的分化能力也伴随着巨大的风险,即其无限增殖的特性可能导致肿瘤形成。此外,ESCs的临床应用还面临两大障碍:一是移植后可能引发的免疫排斥反应;二是其来源涉及人类胚胎,引发了持续且深刻的伦理争议,这为其研究和应用带来了严峻挑战。
诱导多能干细胞:个性化的解决方案与技术的复杂性
诱导多能干细胞(iPSCs)的出现巧妙地规避了ESCs的伦理困境。通过对患者自身的成体细胞(如皮肤成纤维细胞)进行基因重编程,科学家能够获得与ESCs特性相似的多能干细胞。这种“个性化”的细胞来源,使其携带患者自身的基因组,从而显著降低了移植后的免疫排斥风险。
iPSCs在疾病模拟、药物筛选以及神经退行性疾病的治疗研究,特别是分化为多巴胺能神经元方面,显示出巨大价值。尽管优势明显,但iPSCs的重编程和定向分化过程比ESCs更为复杂和低效,其制备技术的安全性和分化效率仍是当前研究需要攻克的关键难题。
间充质干细胞:易于获取的多面手与旁分泌效应
间充质干细胞(MSCs)因其广泛的来源而备受青睐,它们可以从骨髓、脂肪组织以及新生儿脐带等多种成体组织中轻松获得,且伦理争议极小。图2展示了MSCs的分化潜能。
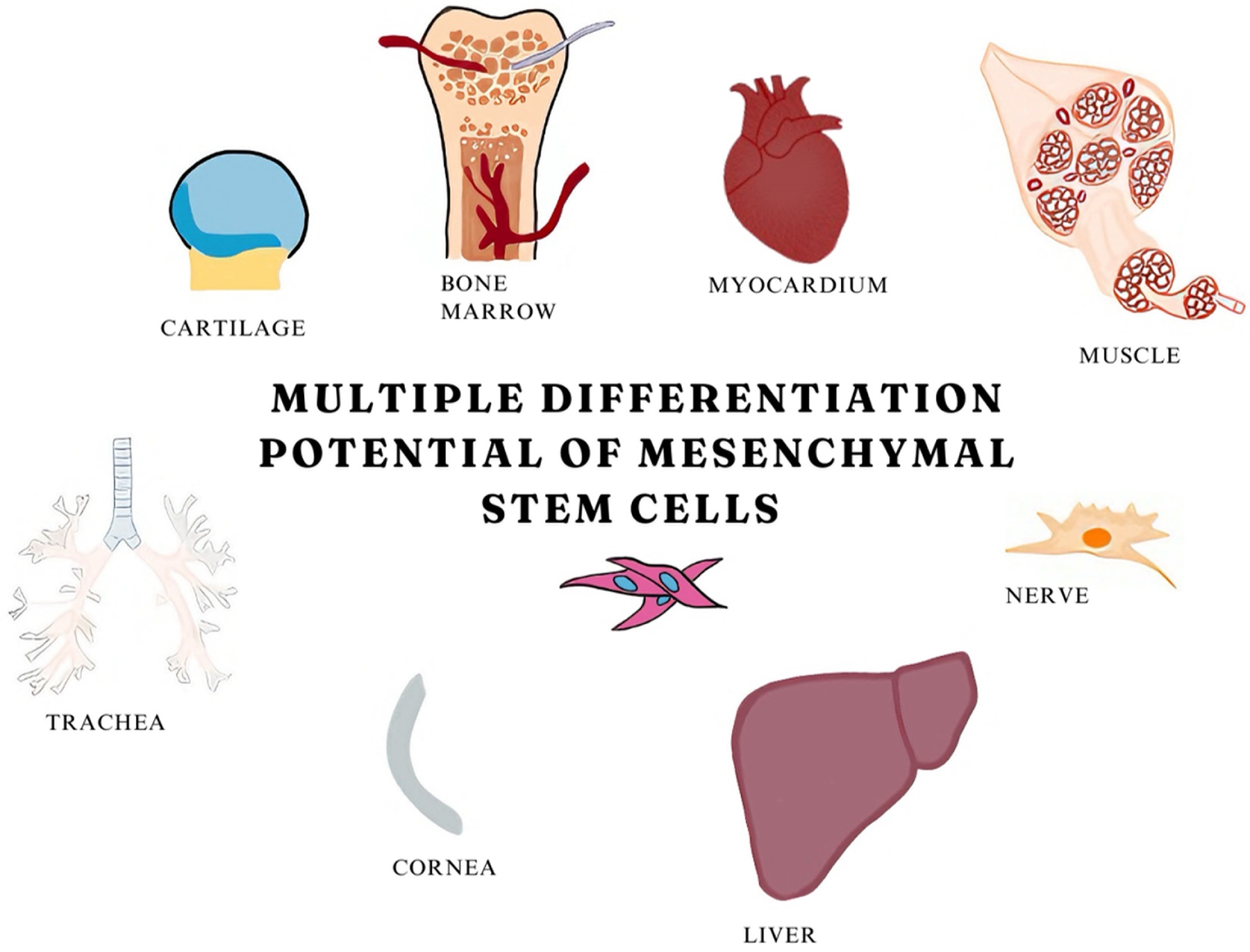
图2:间充质干细胞的分化潜能。
MSCs的优势不仅在于其多向分化潜能和移植后良好的存活率,更在于它们能通过分泌多种神经营养因子,发挥“旁分泌”效应,从而调节免疫反应、保护受损神经元、激活内源性修复机制。在帕金森病和阿尔茨海默病的动物模型中,MSCs已显示出缓解症状和清除致病蛋白斑块的潜力,使其成为一种易于获取且功能多样的治疗工具。
神经干细胞:直接的神经修复者与特定的伦理考量
神经干细胞(NSCs)是专门用于神经系统修复的成体干细胞,它们天然存在于大脑的特定区域,也可以在体外由多能干细胞诱导分化而来。当被移植到体内后,NSCs能够分化为神经元和神经胶质细胞,并通过分泌神经营养因子等活性物质,促进神经环路的修复、增强突触可塑性并改善认知功能,这使其在治疗阿尔茨海默病等神经退行性疾病中显示出直接的治疗优势。
然而,NSCs的传统来源(如胎儿脑组织)同样涉及对胎儿组织的操作,由此引发的伦理问题限制了其广泛应用,促使研究者们寻找更可接受且稳定的替代来源。图3展示了神经细胞的分化途径。
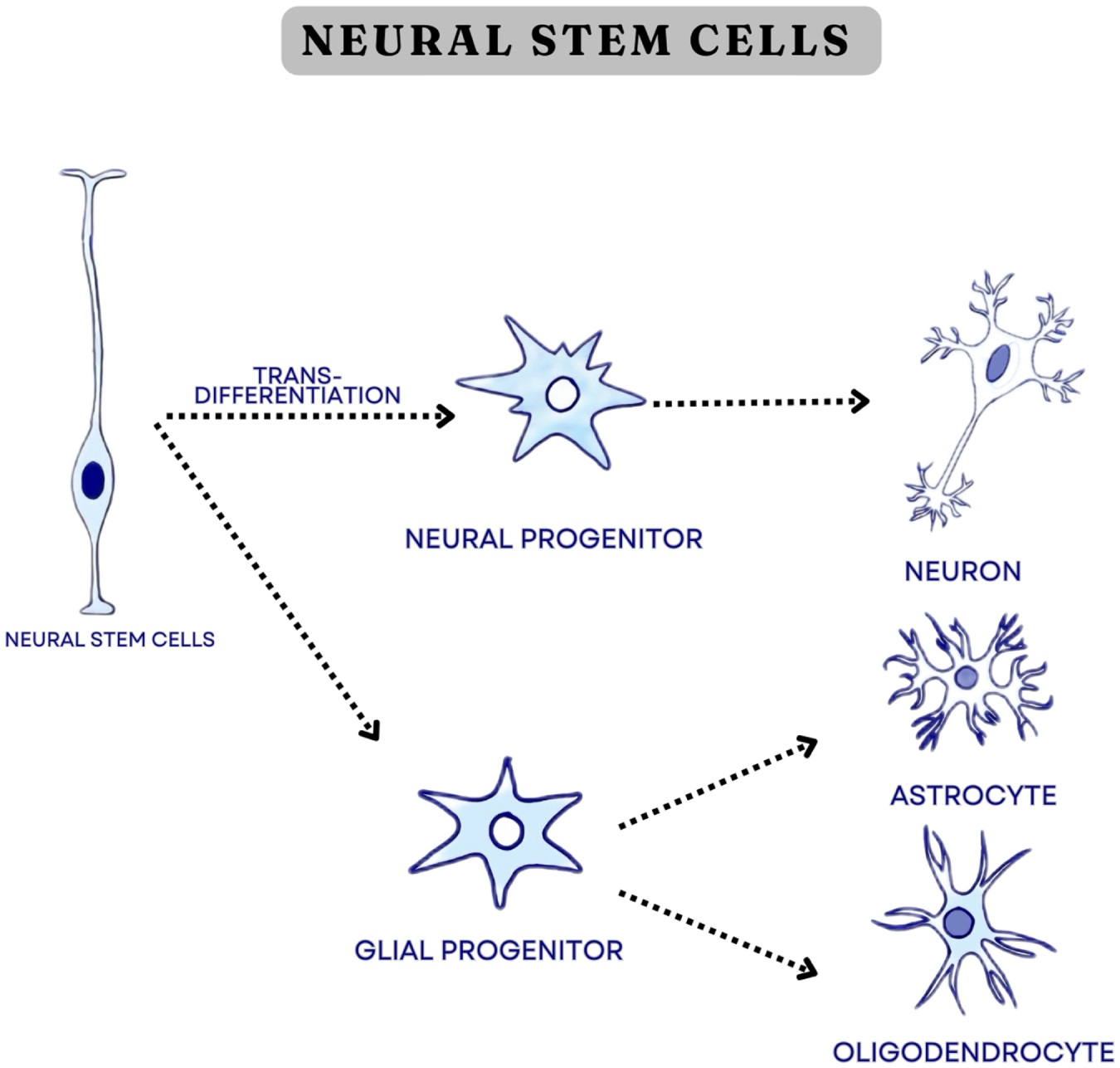
图3:神经细胞分化为神经元、星形胶质细胞和少突胶质细胞的途径。
三、递送方式和移植
干细胞的给药途径包括静脉注射途径(已被证明相对有益);海马内和脑室内注射途径(由于不能进行多次移植,因此不太方便);以及鼻内途径(无创且可重复进行)。
干细胞移植治疗神经退行性疾病的作用机制
干细胞通过多种机制实现神经修复:
- MSCs释放脑源性神经营养因子、胶质细胞源性神经营养因子及神经生长因子,抑制神经细胞凋亡,促进神经发生与血管生成。
- NSCs在中枢神经系统发育中产生神经元与胶质细胞,具备自我更新与修复能力。
- iPSCs可促进神经发生,补偿丢失神经元,且因源自自体细胞,组织排斥风险低于ESC。
- ESCs具有无限分化潜能,可向多谱系分化,但畸胎瘤风险较其他干细胞更高。
表1汇总了各类干细胞疗法的特征及相应临床试验阶段。
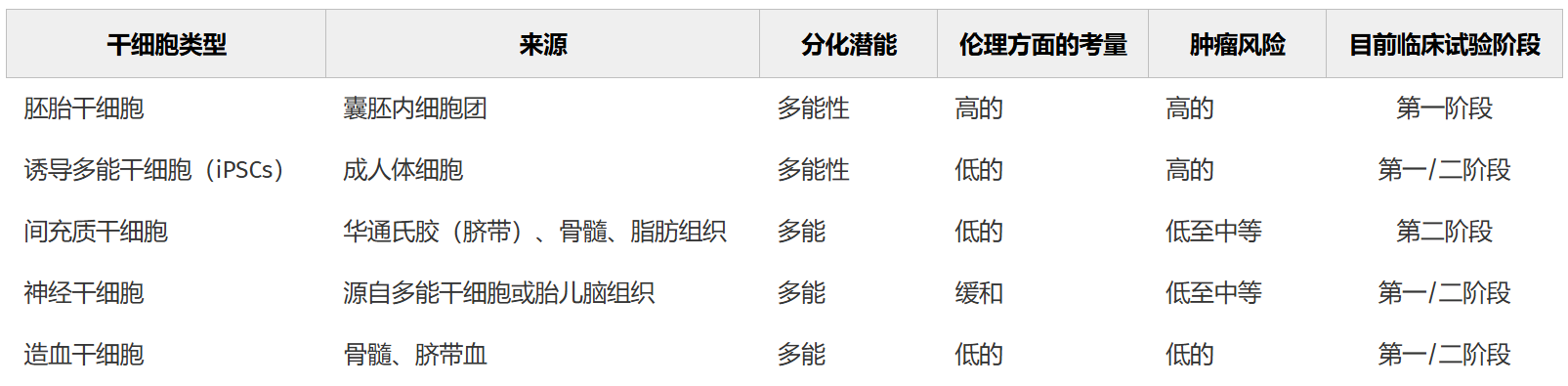
表1:不同干细胞类型及其临床试验阶段的比较总结
五、干细胞治疗四项神经退行性疾病的证据
帕金森病(PD):多能干细胞移植与神经保护因子的探索
针对帕金森病,干细胞治疗的研究重点在于替代受损的多巴胺能神经元。间充质干细胞(MSCs) 因其分泌的外泌体能够穿透血脑屏障并携带多种神经营养因子而备受关注,动物实验证实该方法能有效提高多巴胺水平并保护神经元。
此外,诱导多能干细胞(iPSCs) 的临床转化已进入实质性阶段,京都一项利用同种异体iPSC衍生的多巴胺能神经元移植试验显示,患者未出现肿瘤或移植引起的运动障碍,部分患者甚至观察到运动功能改善,这为多能干细胞(PSCs)疗法的安全性和潜在疗效提供了初步临床证据。
阿尔茨海默病(AD):清除病理蛋白与改善认知功能
在阿尔茨海默病的治疗研究中,干细胞的作用机制主要围绕清除致病蛋白和神经保护展开。
间充质干细胞(MSCs) 被证实能通过增强细胞自噬活性,促进β-淀粉样蛋白斑块的清除。神经干细胞(NSCs) 和诱导多能干细胞(iPSCs) 则在细胞替代方面展现出潜力,能够在动物模型中分化为胆碱能神经元,补充丢失的神经细胞。
尤其值得关注的是,一项通过鼻腔给药的MSC衍生细胞外囊泡(EVs)临床试验观察到,患者的认知功能(通过MoCA和MMSE量表评估)得到改善,这为干细胞衍生产品在AD治疗中的应用提供了直接临床证据。
亨廷顿病(HD):基因矫正与神经前体细胞替代
亨廷顿病是由特定基因突变引起的遗传性神经退行性疾病,其干细胞治疗策略强调细胞替代与基因矫正的结合。目前首选的是神经干细胞(NSCs),它们可以来源于胚胎干细胞或诱导神经干细胞(iNSCs),并在动物模型中展现出治疗潜力。
针对该病特有的CAG重复序列突变,研究者正尝试将干细胞技术与基因编辑(如CRISPR/Cas9) 结合,以在移植前修复或替换突变基因。此外,间充质干细胞(MSCs) 也通过增强线粒体功能和促进神经生成,在缓解疾病进程中发挥辅助作用。
肌萎缩侧索硬化症(ALS):运动神经元再生与病理挑战
肌萎缩侧索硬化症以运动神经元的进行性死亡为特征,干细胞治疗的目标是再生功能性运动神经元并调节致病微环境。胚胎干细胞(ESCs) 因其能分化为运动神经元并改善动物模型的运动功能,被视为潜在的治疗工具。神经干细胞(NSCs) 同样可以体外生成运动神经元,并能与肌肉纤维形成功能性突触,为神经再支配提供了可能。
尽管该病的发病机制复杂(涉及神经元和胶质细胞的相互作用),给治疗带来更大挑战,但临床观察显示,接受干细胞治疗后患者脑脊液中的特定生物标志物水平有所下降,提示干细胞疗法在改变疾病进程方面具有潜在价值。
六、干细胞移植治疗神经退行性疾病近期的临床试验
表2列出了临床试验的结果,该表已纳入本研究。它涵盖了正在评估用于治疗各种神经退行性疾病的多种干细胞类型。部分临床试验仍在进行中,由于结果尚未公布,因此表中仅列出了预期结果以及待评估/测量的指标。这些临床试验的结果对于确定干细胞疗法在神经退行性疾病患者中的安全性、有效性和合适剂量至关重要。
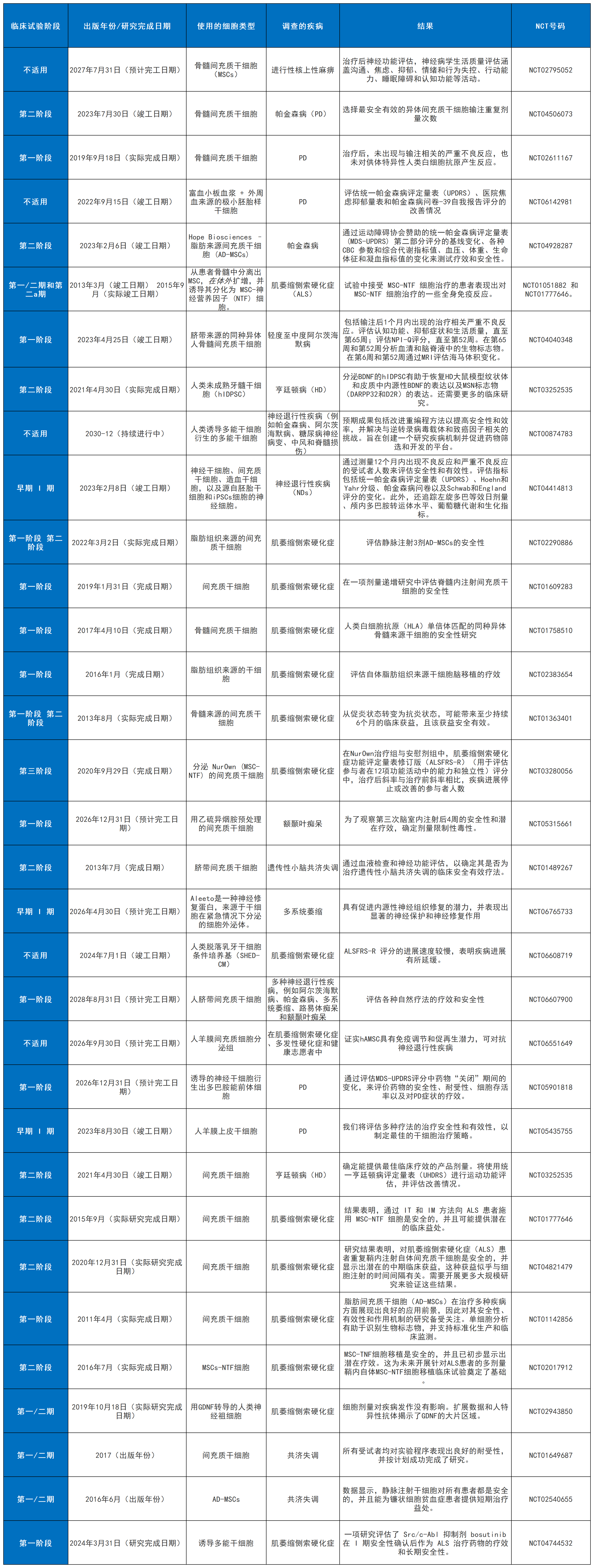
表2:间充质干细胞疗法治疗神经退行性疾病的临床试验概述。
干细胞移植治疗神经退行性疾病新药上市的障碍分析
(一)临床前与临床研究之间的“转化鸿沟”
尽管大量动物实验和临床前研究展现了令人鼓舞的前景,但这些结果往往难以在人体临床试验中复现。这种不可靠性构成了干细胞疗法转化的首要障碍。此外,临床试验本身的开展也充满挑战,例如立体定向注射等移植手段可能引发患者的呼吸问题,研究方案缺乏统一规范,以及资金不足、新冠疫情等外部因素都可能导致试验失败或中断。要从实验室成功走向临床应用,必须严格遵守监管机构制定的复杂指南,而这并非易事。
(二)严格的监管审批与法规不确定性
美国食品药品监督管理局(FDA)和欧洲药品管理局(EMA)等监管机构为保障患者安全,制定了极为严格的干细胞分离、制备和移植指南,要求采用完全标准化的方案。这本身就是一个耗时且成本高昂的过程。更关键的是,干细胞疗法的监管分类尚不明确——它究竟属于药品还是生物制品?这种不确定性使得研发机构在申请许可和走完审批流程时面临更大的困难。
迄今为止,监管机构仅正式批准了少数来源明确、用途特定的干细胞(如造血干细胞),而针对神经退行性疾病的复杂干细胞产品尚未达到其严苛的上市标准。
(三)不受监管的干细胞诊所对行业的冲击
在全球范围内,有数百至上千家不受监管的诊所,利用患者的急切心理,提供未经证实、未经标准化的所谓“干细胞治疗”。这些机构提供的细胞制剂既没有经过严格的安全评估,制备过程也不规范,导致患者在接受治疗后出现了肿瘤、感染等严重不良反应。这不仅直接损害了患者的健康,也破坏了干细胞疗法在公众中的声誉。这种乱象还干扰了正常的科研和审批秩序,迫使监管机构投入更多精力进行打击和规范,间接延缓了正规疗法的上市进程。
结论
神经退行性疾病以神经元渐进性退变为核心,常伴随多重症状与运动障碍。传统放疗、手术与康复手段仅能缓解症状,干细胞疗法则为治疗开辟了新路径。ESCs、iPSCs、MSCs与NSCs各具优势与局限;MSCs来源外泌体在AD与PD治疗中亦展现出良好前景。然而,免疫排斥、肿瘤风险与伦理争议仍是亟待突破的瓶颈。递送系统与纳米技术的进步,有望提升治疗的安全性与有效性,为临床转化铺平道路。
本综述系统梳理了近年来干细胞治疗神经退行性疾病的研究进展与临床试验证据,弥合基础科学与转化医学之间的鸿沟。通过聚焦创新递送方法、基因修饰策略及伦理考量,本文为未来研究与临床实践提供了切实可行的参考,助力推动该领域迈向规范、安全、高效的发展轨道。
参考资料:
[1]:帕特尔,Tirath AS,BS,MS a,*;指甲花,Fathimathul MBBS b;谢里夫,伊曼 MBBS c;Javed,Inaya MBBS c;穆斯塔法,法蒂玛 MBBS c;谢里夫,汉南 MBBS c;纳西尔·法蒂玛 MBBS c;Javaid、Mirat MBBS c;萨曼·法蒂玛·乌斯曼 MBBS d;克里斯托弗·哈纳尼(Hanani )阿南德(Anand),尼基莱什(Nikhilesh)医学博士。干细胞在神经退行中的治疗中的应用:进展、态度与挑战——综述。 《内科与外科年鉴》88(2):1441-1453页,2026年2月。数字编号: 10.1097/MS9.0000000000004490
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。
郑重声明:本文版权归原作者所有,转载文章仅为传播更多信息之目的,如作者信息标记有误,请第一时间联系我们修改或删除,多谢。




发表回复