卵巢衰老标志——卵母细胞数量减少和质量下降
女性的生殖潜能根本上取决于卵巢中卵母细胞的数量与质量,这两者均随年龄增长而呈现协同性衰退。卵巢储备(数量)自胎儿期起便持续不可逆地消耗,而卵母细胞的发育潜能(质量)则在30岁后出现显著下降。这两个并行且相互关联的生物学过程是卵巢衰老标志,共同绘制了女性生育力的自然衰减曲线,并对生殖医学提出了核心挑战。
一、 数量标志:卵巢储备的不可逆衰减
卵母细胞的数量储备是一个从顶峰持续下滑的过程。女性胎儿在妊娠中期,原始卵泡数量达到约700万的峰值。然而,自出生起,这一储备便通过闭锁机制不断耗减:新生儿期降至100-200万,青春期约剩40万,在整个生育期内仅有约400个卵泡最终排卵。数学模型揭示,卵巢储备的消耗呈非线性加速,尤其在30岁左右后下降曲线更为陡峭,这主要由卵泡闭锁率增加驱动。直至绝经时(平均年龄51岁),卵巢中仅存不足1000个原始卵泡,标志着生殖潜能的生理性终结。因此,原始卵泡数量的动态变化是衡量卵巢早衰最基础的数量标志(图1)。
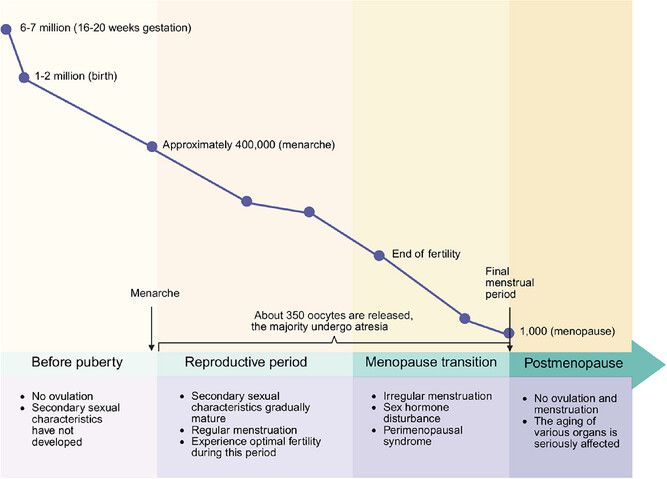
图1:卵巢的生命周期。图示展示了卵巢在不同生命周期阶段的变化,从青春期前到绝经后,卵泡数量和卵巢功能的动态变化。
二、 质量标志:细胞功能与发育潜能的衰退
在数量减少的同时,卵母细胞的质量也在经历深刻的、与年龄相关的功能退化。这一过程大约从31岁后开始变得明显,并与储备下降同步加速。质量衰退不仅直接导致生育力下降和流产率升高,也影响内分泌稳态。
1. 核心细胞机制缺陷: 在细胞层面,衰老卵母细胞表现为:减数分裂纺锤体组装紊乱,导致染色体非整倍体率急剧上升;线粒体功能障碍与DNA损伤累积,造成能量供应不足和基因组不稳定;以及端粒缩短等。其中,线粒体DNA突变积累是质量下降的关键驱动因素,它损害了卵母细胞完成成熟、受精和早期胚胎发育所需的能量与调控基础。
2. 评估方法的演进:从形态到功能: 传统辅助生殖技术依赖形态学评估(如极体、透明带),但其预测价值有限。现代评估更注重功能性指标:线粒体膜电位(ΔΨm) 能直接反映卵母细胞的代谢活性与发育潜能;生发泡期染色质构型(如SN型)可预测核成熟同步性。整合这些功能参数,能实现更精准的胚胎选择。
3. 微环境的关键作用:颗粒细胞功能衰退: 卵母细胞的质量与其周围的颗粒细胞密不可分。卵巢衰老时,颗粒细胞出现显著的线粒体功能减退、代谢通路异常(如甲羟戊酸途径抑制)和氧化应激加剧。这些变化削弱了其对卵母细胞的营养支持与信号调控,直接导致后者质量下降。研究证实,恢复颗粒细胞功能或利用年轻颗粒细胞共培养,可部分逆转卵母细胞的衰老表型,这凸显了卵泡微环境健康是评估卵母细胞质量不可或缺的维度。
三、 总结与展望
综上所述,卵巢早衰的核心标志体现在卵母细胞数量的耗竭与质量的退化两个方面,二者相辅相成,共同决定生殖结局。当前,对质量评估正从静态形态学转向动态功能学,并日益重视卵泡微环境的作用。未来,通过整合数量储备(如AMH、AFC)与质量功能(如线粒体活性、颗粒细胞状态)的多维生物标志物,将能更早、更精准地评估卵巢年龄,并为开发针对性的干预措施(如改善线粒体功能、调节颗粒细胞代谢)提供科学依据,从而在生殖医学和女性健康衰老领域实现突破。
郑重声明:本文版权归原作者所有,转载文章仅为传播更多信息之目的,如作者信息标记有误,请第一时间联系我们修改或删除,多谢。
发表回复