脊髓损伤(SCI)是一种毁灭性的中枢神经系统创伤,通常由外部机械力导致脊髓结构受损,引发损伤平面以下运动、感觉及自主神经功能障碍。全球有超过1500万患者深受其害,中国患者人数估计超过300万,且每年新增约10万病例。SCI不仅造成患者终身残疾,还带来巨大的心理负担和社会经济压力。
传统治疗手段如手术减压、药物和康复训练,虽能在一定程度上稳定脊柱、减轻继发损伤并改善部分功能,但均无法实现神经结构的真正再生和功能的完全恢复。血脊髓屏障的存在限制了药物递送,而中枢神经系统固有的低再生能力更使修复困难重重。
面对这一困境,干细胞疗法凭借其独特的自我更新、多向分化和分泌调节能力,成为再生医学领域最具前景的治疗方向。间充质干细胞治疗脊髓损伤、神经干细胞治疗脊髓损伤是当前脊髓损伤临床研究的两大主流策略,二者分别通过独特机制促进神经修复,为脊髓损伤患者的功能恢复带来了新的希望。那么这两种疗法,哪种更适合特定类型的脊髓损伤患者?我们该如何科学选择呢?本文将围绕二者治疗脊髓损伤的具体作用机制、临床研究证据与适用场景,逐一深入解析,帮助读者对两种疗法形成理性判断,为实际治疗决策提供参考。
间充质干细胞治疗脊髓损伤更有效?还是神经干细胞?
一、干细胞类型概述
1.1 间充质干细胞
来源:MSCs是一种中胚层来源的多能成体干细胞,获取来源广泛,包括骨髓、脂肪组织、脐带和胎盘等。其中,脐带来源的MSCs(UC-MSCs)因增殖能力强、免疫原性低且无伦理争议,在临床应用中备受青睐。
基本特性:MSCs的核心优势并非直接分化为神经细胞,而在于其强大的免疫调节和旁分泌功能。它们能分泌多种神经营养因子(如BDNF、GDNF)、抗炎因子(如IL-10)和促血管生成因子(如VEGF),从而改善损伤微环境、抑制凋亡、促进内源性修复。此外,MSCs易于在体外扩增,可进行自体移植,避免了免疫排斥问题
1.2 神经干细胞
来源:NSCs是存在于神经系统中的一类干细胞,可直接从胎儿脑或脊髓组织中获取。然而,随着重编程技术的发展,通过诱导多能干细胞(iPSCs)定向分化为NSCs已成为主流趋势,这不仅解决了伦理问题,还为实现“现货型”细胞治疗提供了可能。
基本特性:NSCs的核心能力是多向分化潜能,它能直接分化为构成神经系统的三大类细胞:神经元、星形胶质细胞和少突胶质细胞。因此,NSCs移植旨在直接替代受损的神经细胞,重建神经环路,并促进髓鞘再生以恢复信号传导。
| 特性 | 间充质干细胞(MSC) | 神经干细胞(NSC) |
|---|---|---|
| 主要来源 | 骨髓、脂肪、脐带 | 胎儿神经组织、iPSC分化 |
| 分化潜能 | 有限神经分化,主要分化为支持细胞 | 可分化为神经元、星形胶质细胞、少突胶质细胞 |
| 主要机制 | 免疫调节、分泌神经营养因子、促进血管生成 | 替代受损神经元、重建神经网络、形成髓鞘 |
| 优势 | 免疫原性低、易于获取、安全性较好 | 神经定向分化能力强、整合效率高 |
| 局限性 | 神经分化能力有限 | 来源受限、伦理争议 |
二、作用机制对比
2.1 间充质干细胞的主要作用机制
MSCs治疗脊髓损伤的主要机制不仅限于分化替代,而是通过多重旁分泌效应实现:
抗炎作用:调节小胶质细胞从促炎M1型向抗炎M2型转化,降低肿瘤坏死因子-α(TNF-α)和白介素-1β(IL-1β)等炎性因子水平,减轻继发性损伤;
分泌生长因子:产生多种神经营养因子,如BDNF、GDNF和NGF,促进神经元存活和轴突再生;
促进血管生成:通过分泌VEGF和Angiopoietin-1等因子,改善损伤局部血液供应,为神经修复提供营养支持;
减少细胞凋亡:抑制Caspase-3等凋亡相关蛋白表达,保护受损但尚未死亡的神经细胞。
2.2 神经干细胞的主要作用机制
NSCs则主要通过直接替代和结构重建发挥作用:
替代受损神经元:分化为功能性神经元,替代因损伤而死亡的神经细胞,直接参与神经信号传导。研究表明,移植的NSCs可分化为运动神经元(占16%)、V2中间神经元(占11%)和dI4中间神经元(占29.4%)等多种功能细胞;
促进神经网络重建:延伸神经纤维与宿主神经元形成突触连接,重建神经信号通路。免疫荧光染色证实,移植细胞表达的人特异性突触蛋白(hSyn)与宿主神经标志物(MAP2)存在共定位,表明真正实现了”信号互通”;
形成髓鞘:分化为少突胶质细胞,包绕受损轴突形成髓鞘,恢复神经传导速度;
调节微环境:最新研究发现,NSCs同样具有调节损伤局部微环境的能力,可抑制胶质瘢痕形成,为轴突再生”打开通道”。
三、临床与实验研究数据证据对比
3.1 间充质干细胞治疗脊髓损伤患者的临床数据
2025年3月6日,“国家两委备案干细胞临床研究·脊髓损伤患者招募”媒体发布会召开,西安医院正式启动了西北地区首个中枢神经损伤干细胞项目。该项目旨在通过间充质干细胞移植治疗脊髓损伤,标志着从“不可逆”损伤到“功能重建”的重要临床突破。[1]

在发布会上,院长详细介绍了“间充质干细胞移植治疗脊髓损伤”项目的申报背景及过程。他指出,试了手术、药物等很多方法,多年来病情始终没有进展,停留在同一疗效上。传统治疗手段仅能通过手术减压清理损伤部位,却无法实现神经信号通路的再生修复。
基于此,贺院长带领团队开启了干细胞疗法的研究,希望通过精准的干细胞移植技术,重建受损神经系统的“通信网络”,为患者提供新的治疗途径。
张伟主任在会上分享了项目的初步成果:参与临床研究的6名脊髓损伤患者中,5例患者出现了神经功能的改善,4例患者运动功能显著提升,其中2例患者的恢复情况尤为突出。一位完全性损伤患者在接受治疗后,已经能够在辅助下短暂站立,这表明细胞移植治疗脊髓损伤具有可行性,并为进一步的临床试验提供了有力依据。
山西一名22岁的脊髓损伤患者,因高空坠落后只能坐轮椅,下肢持续打颤抽动,连在床上坐都困难。进行了干细胞移植术后,下肢肌肉逐渐有劲,现在已经能自行滚背和跪立了。
另一位脊髓损伤患者,平时走路只能借助于拐杖,在细胞移植术后一个月,他已经能扔掉拐杖轻松走路了。

3.2 神经干细胞移植治疗脊髓损伤患者的临床数据
2024年12月17日,加州大学圣地亚哥分校医学院研究人员在行业期刊《细胞医学报告》上发表了一篇关于《神经干细胞移植治疗慢性胸椎损伤的单中心Ⅰ期临床研究》的长期临床和安全性结果。[2]
本次发布的I期临床研究旨在评估神经干细胞移植治疗慢性胸椎脊髓损伤的安全性和初步疗效。研究选取了四名完全性ASIA-A级胸部SCI患者作为受试者,这些患者的损伤时间均超过一年,且在接受任何其他形式的有效治疗后仍未见明显好转。

每位受试者接受了每个注射点含有2×105个神经干细胞,通过定制的立体定向设备,双侧注入损伤部位周围的剩余组织及下方约一个节段的内侧白质区,整个过程由术中荧光透视成像指导完成。
临床结果:
1.神经系统反应概览:按ISNCSCI随访,2名受试者(001、010)在移植后出现了明显的神经学改善:001在移植后2年曾上升两个节段,5年回落至上升1个节段;010则在整个5年随访期间保持了稳定的神经功能提升。
2.免疫抑制与免疫反应:四名受试者均在移植后12周停用他克莫司和霉酚酸酯;虽有一例(010)在6个月检测到阳性抗HLA抗体,但并非针对供体特异性抗体,研究组认为这并非由NSC移植直接引起的免疫排斥反应。
3.疼痛与生活质量:疼痛方面,001和006报告总体疼痛下降,008疼痛加重且因骶骨溃疡在30个月时发生严重不良事件导致生活自理能力(SCIM)明显下降,010的疼痛和SCIM变化较小,总体3名患者SCIM未见显著改善。
4.影像学评估:术后MRI显示所有患者存在不同程度的局灶性脊髓软化,但未见新的并发影像学征象(如水肿、增强或积液);DTI提示脊髓束外观稳定,未见广泛重塑或纤维束改善。
5.神经生理反应:电生理检查显示多名患者在移植后数月至数年间出现新的肌电活动与对强化动作的反应(例如001、006、010在不同节段出现新发EMG信号和增强的肌肉反应),提示部分节段出现了功能性神经肌肉恢复迹象。
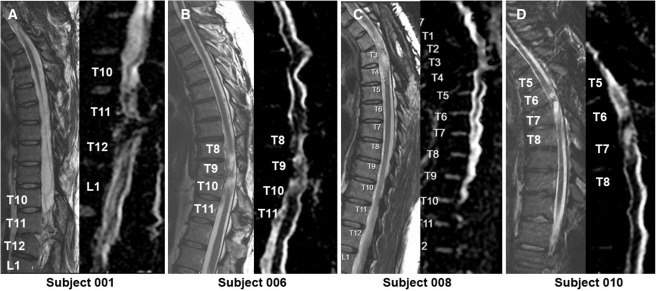
研究结果表明,神经干细胞移植是一种可行且相对安全的方法,能够在一定程度上促进慢性胸椎SCI患者的神经功能恢复。
2025年7月2号,美国加州大学圣地亚哥分校神经科学系在国际权威期刊杂志《Translational Neuroscience》发表了一篇“神经干细胞治疗脊髓损伤”的文献综述。[3]

该综述研究表明:神经干细胞或神经祖细胞 (NPC) 移植到严重脊髓损伤 (SCI) 部位后能够存活,分化为神经元和神经胶质细胞,并延伸出大量轴突,延伸至相当长的距离,以便与损伤部位下方的宿主神经元建立连接。反过来,宿主的轴突会再生到NSC/NPC移植物中,并与移植物来源的神经元形成突触连接。
因此,NSC/NPC移植物来源的神经元可以作为神经元中继,重建损伤部位的神经传递,即使在严重SCI后也能改善功能结局。
3.3 直接对比与综合分析
目前极少有头对头比较MSCs和NSCs疗效的临床研究。但从现有数据看:
安全性:MSCs的临床安全性记录更为丰富和成熟,应用也更简便(可静脉/鞘内给药)。NSCs的移植通常需要精准的病灶内注射,操作更具侵入性,且其长期安全性(如致瘤性)仍需更多数据评估。
有效性:MSCs在调节免疫微环境、保护残存神经组织方面表现突出,尤其在急性期和亚急性期。而NSCs在结构重建(细胞替代) 方面潜力更大,其能够直接替代受损神经元,重建神经网络,突破胶质瘢痕的阻碍,对慢性期患者更有利。
功能恢复效果方面:MSCs主要改善ASIA评分和体感诱发电位,但对某些神经功能影响有限;而NSCs则可带来更全面的感觉与运动功能改善,包括精细运动控制和步态协调性。
总结与展望
综合现有证据,间充质干细胞和神经干细胞在治疗脊髓损伤方面各具优势,其适用性取决于损伤阶段、损伤类型和治疗目标。MSCs擅长在急性期调控炎症、改善微环境;NSCs则在慢性期神经替代与回路重建上潜力更大。未来治疗趋势是发展联合策略,并结合基因工程、3D支架等新技术,最终为患者实现有意义的功能恢复。
郑重声明:本文版权归原作者所有,转载文章仅为传播更多信息之目的,如作者信息标记有误,请第一时间联系我们修改或删除,多谢。



发表回复