自20世纪60年代起,Carlsson、Hornykiewicz、Cotzias和Yahr发现帕金森病(PD)患者黑质多巴胺缺乏,并引入了多巴胺替代疗法以来,大量药物和神经调控治疗已有效缓解运动症状。在再生医学领域,PD一直是细胞治疗的关键目标,旨在改善症状并实现疾病修饰,过去几十年里已在临床上探索了多种方法。
细胞治疗帕金森病的两大策略:移植与输注的利弊
PD的干细胞治疗主要遵循两大策略:细胞移植和静脉输注(IV)。细胞移植是研究较为广泛的方法,旨在将干细胞分化为多巴胺能神经元,以直接恢复神经递质传递。然而,该方法存在诸多局限,包括细胞来源的伦理问题、手术植入的侵入性、潜在的肿瘤形成风险、免疫原性以及移植物诱导的运动障碍等,这些因素共同限制了其在轻中度PD患者中的应用。
相比之下,间充质干细胞(MSCs)的静脉输注逐渐成为一种更具前景且安全的治疗选择。这类细胞因其强大的免疫调节功能而受到关注,能够通过调节外周免疫系统来改善PD的核心病理环节——神经炎症。此外,MSCs还具有免疫原性低、致瘤风险小、易于从多种组织中获取并实现规模化生产、伦理争议较少等综合优势。
间充质干细胞治疗帕金森病的作用机制:系统性免疫调节与神经营养支持
在PD动物模型中,MSCs被证明可通过多靶点机制减少小胶质细胞活化,并促进多巴胺神经元存活。虽然有研究表明,MSCs可能迁移至黑质并通过与多巴胺能细胞直接相互作用抑制小胶质细胞活化,但由于其直径(15–30μm)较大,约80%–90%会被困在肺部狭窄的毛细血管中,因而直接植入极为罕见且短暂。
其核心作用机制在于系统性免疫调节和神经营养支持。目前认为,MSCs或其分泌体(如细胞外囊泡和外泌体)作为“微工厂”发挥作用,通过释放抗炎细胞因子(如TGF-β、IL-10、PGE2)来调节全身免疫反应,并可能降低血脑屏障的通透性。
同时,它们还能分泌多种神经营养因子(如BDNF、GDNF、NGF),从而促进神经元存活、修复与突触可塑性。在PD动物模型中,MSCs被证实可通过这些多靶点机制抑制小胶质细胞活化,并支持多巴胺能神经元存活,从而有望干预疾病的病理进程。
从理论到实践:I期临床研究启示与II期试验设计
基于上述理论,美国德克萨斯大学麦戈文医学院(以下简称“我们”)于2021年开展了一项I期单剂量递增试验,采用来自健康供体的同种异体骨髓来源MSCs(allo-hMSCs)。该策略充分利用了“现成”同种异体细胞的优势,包括可实现大规模生产、无需进行患者个体化的细胞采集,以及能提供更年轻、活性更高的细胞,从而减少因供体衰老带来的潜在风险[1]。

试验结果显示,在轻中度PD患者中,单次静脉输注1–10×10⁶allo-MSCs/kg剂量安全且耐受良好,未引发免疫原性反应。探索性分析表明,接受最高剂量(10×10⁶cells/kg)的患者在输注后3、12、24及52周的“停药”状态下,其统一帕金森病评定量表(UPDRS)运动评分均显示改善,并且症状获益随时间保持稳定。
基于这些鼓舞人心的结果,并结合帕金森病慢性进展的特性,我们提出假设:反复输注最高安全剂量的allo-hMSCs可能会增强和维持其免疫调节效应,从而带来更显著、更持久的临床症状改善。
为验证该假设,我们牵头开展了一项II期双盲、随机、安慰剂对照试验,旨在评估重复allo-hMSC输注对改善PD患者运动及非运动症状的疗效。(研究结果发表在期刊杂志《运动障碍主页》上)[2]。

II期临床试验概况
研究设计与方法:在这项II期随机安慰剂对照试验(2020年11月至2023年7月)中,轻度至中度帕金森病患者接受三次异基因hMSC输注,一次安慰剂输注后再进行两次异基因hMSC输注,或以18周为间隔进行三次安慰剂输注,随访持续88周。
主要结局指标为第62周时,在停药后运动障碍协会主办的统一帕金森病评定量表第三部分修订版(MDS-UPDRS-III)中,患者比例改善≥5分的后验概率(PP)差异是否大于70%。使用Rv4.2.0进行贝叶斯分析。
试验人群:总共有160名患者接受了预筛选,49名接受了筛选,45名最终入组。其中,16名接受了三次异基因hMSC输注,14名接受了一次安慰剂输注,随后又接受了两次异基因hMSC输注,15名接受了三次安慰剂输注。基线人口统计学和临床特征见表1。
到第62周,42名患者完成了所有输注和评估;两名患者退出,一名患者在被诊断为多系统萎缩(经αSyn-SAA证实)后被排除在外。另外两名患者因不相关的健康问题停止研究,剩下40名患者完成了88周的随访(图1)。
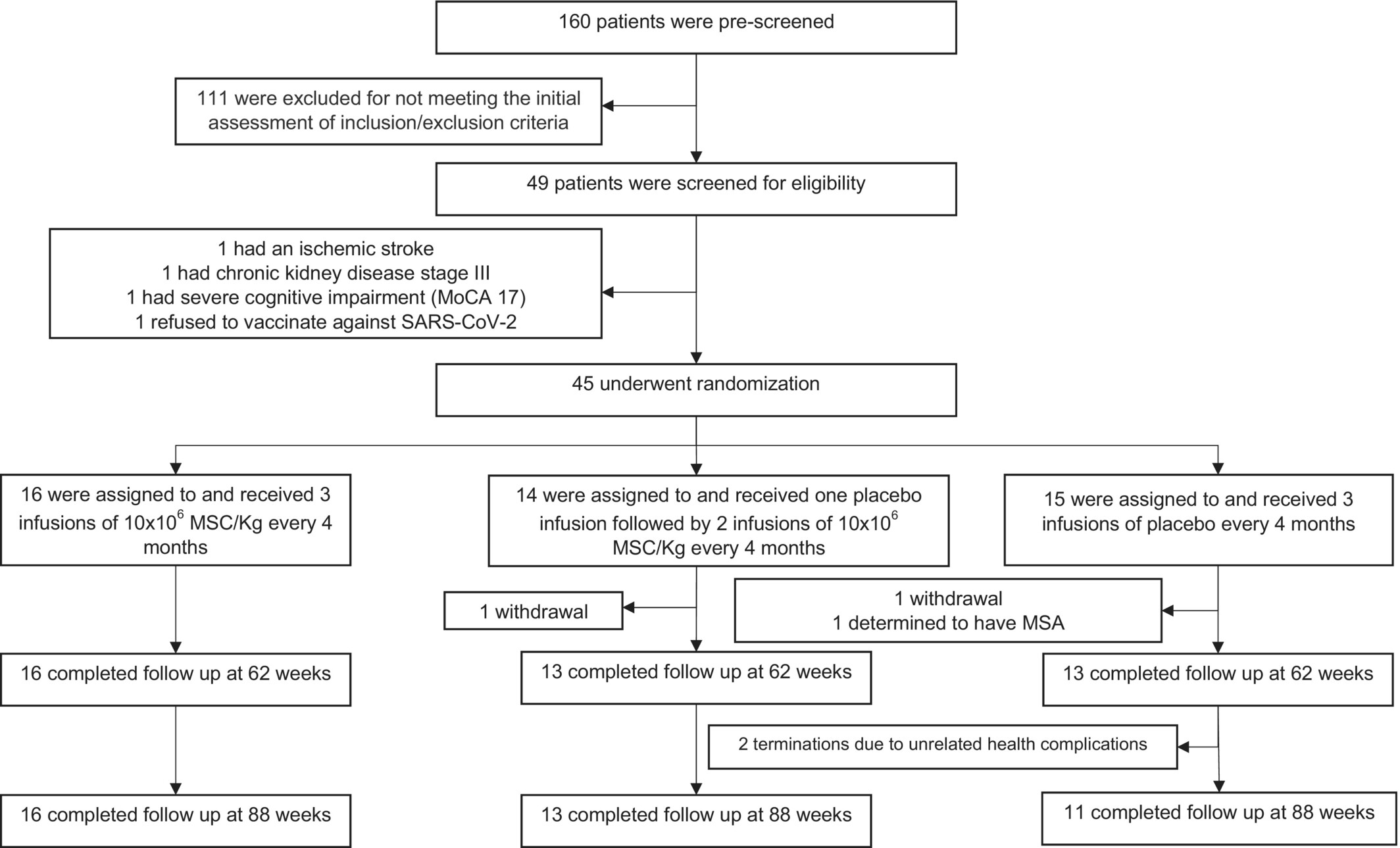
图1:研究流程
同种异体骨髓间充质干细胞治疗帕金森病的主要结果
第62周运动症状改善的组间差异
三次输注在第62周的临床重要改善:第62周时,三次输注组中MDS-UPDRS-III运动评分改善≥5分的受试者比例与安慰剂组相比有所增加(图2A)。使用更严格的阈值(≥11分),三次输注组中改善的受试者比例与安慰剂组相比有所增加(图2B)。
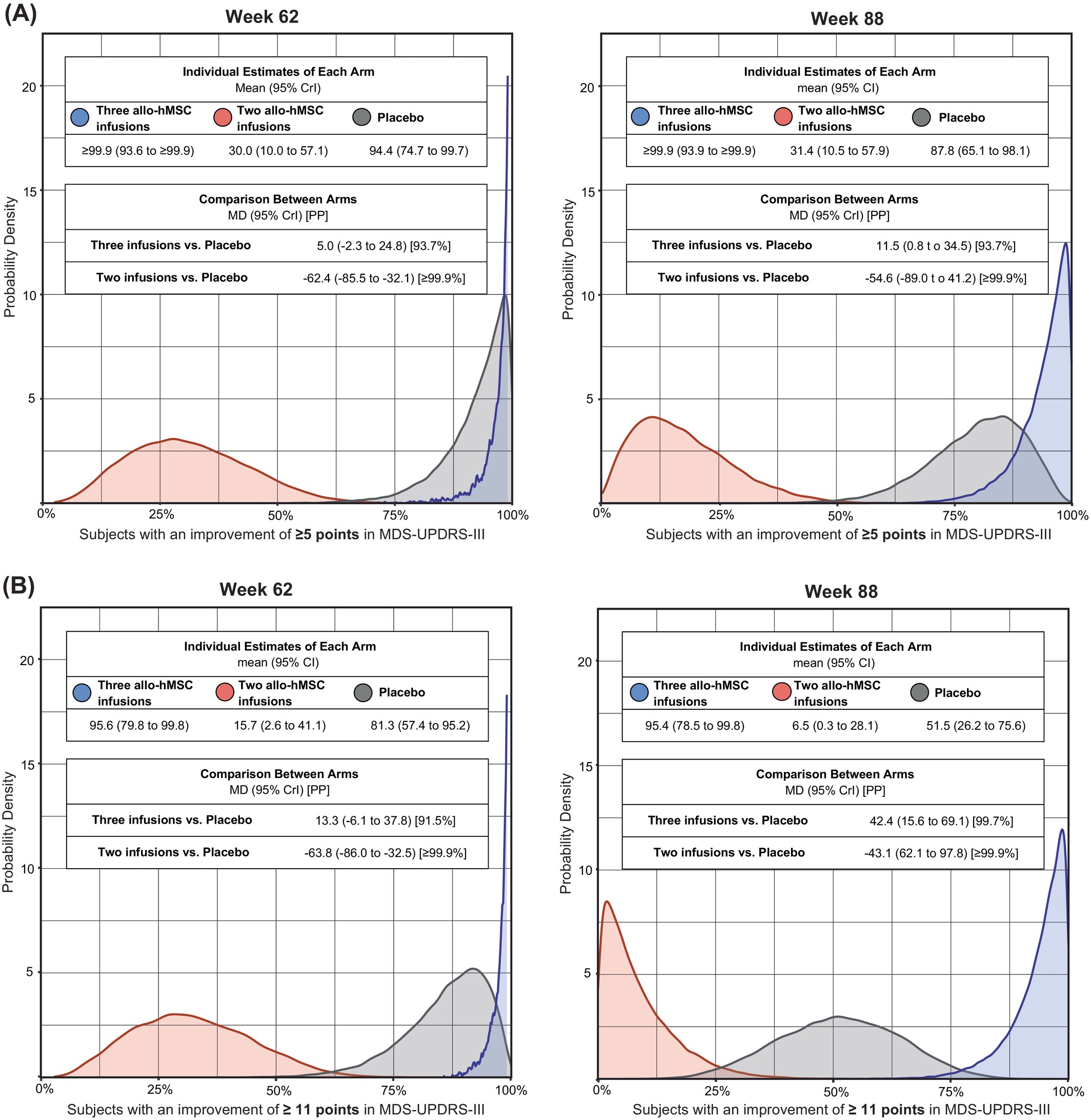
图2:接受人同种异体骨髓间充质干细胞 (allo-hMSCs) 治疗后,帕金森病患者在运动障碍协会主办的统一帕金森病评定量表第三部分修订版 (MDS-UPDRS-III) 评分中获得中度或较大临床重要性改善的比例。
两次输注组的负面疗效表现:相反,与安慰剂组相比,两次输注组中达到≥5分(图2A)和≥11分(图2B)阈值的受试者较少。虽然置信区间存在一定交叉,但总体趋势支持三次输注方案的潜在获益。
同种异体骨髓间充质干细胞治疗帕金森病的次要结局
其他次要临床结局的结果,包括从基线起MDS-UPDRS各部分(I、II、III、IV)、总分、PDQ-39以及EQ-5D-5L指数评分的变化,见表2。
MDS-UPDRS-III评分变化趋势:从基线到第88周
至第62周,三次输注组评分较基线改善16.9分,接近安慰剂组的14.6分改善,两组间差异仅为2.3分。而两次输注组仅改善3.9分,显著劣于安慰剂组(组间差异+20.6分)。这一趋势持续至第88周,三次输注组优势扩大至3.3分(表2)。各访视时平均MDS-UPDRS-III评分的变化汇总于图3。
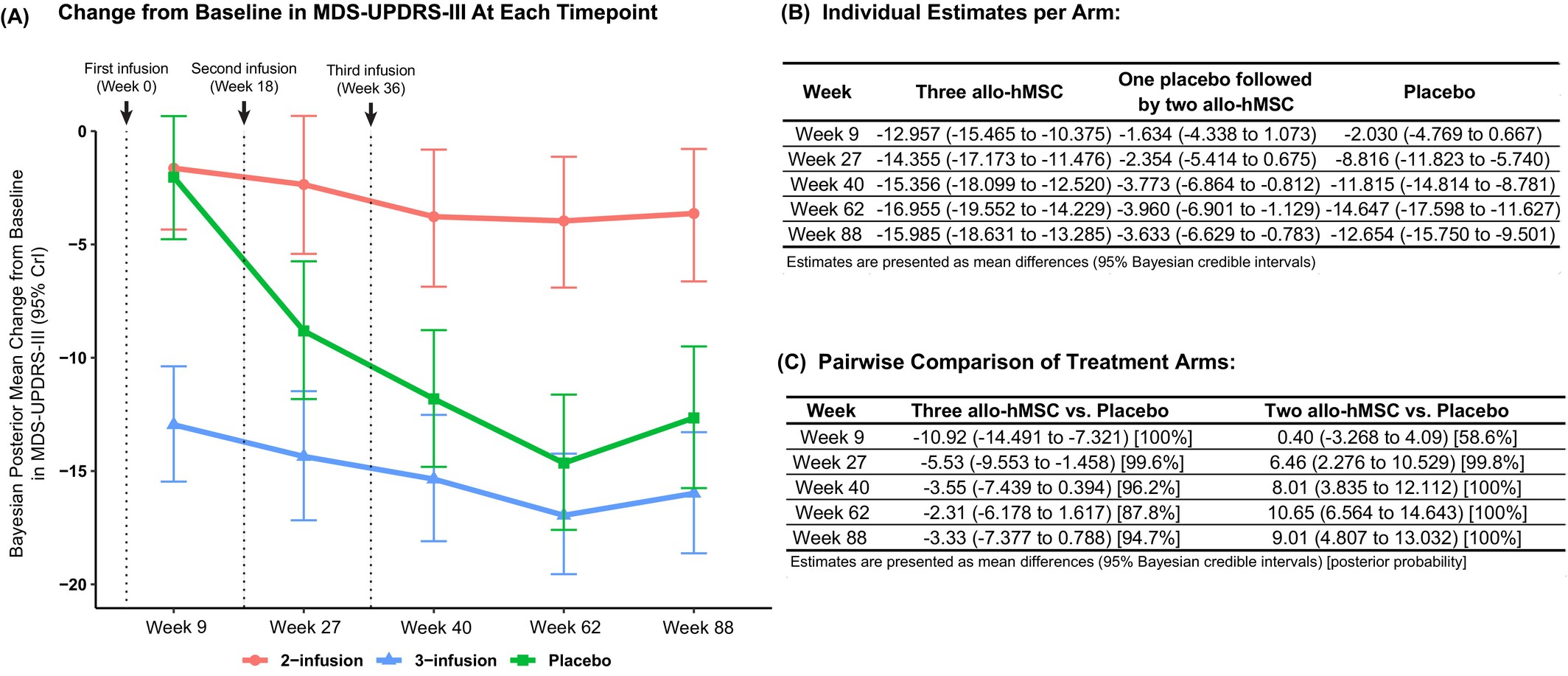
图3:运动障碍协会主办的统一帕金森病评定量表第三部分 (MDS-UPDRS-III) 修订版各治疗组的改善轨迹。
长期疗效:第88周临床差异持续扩大
在第88周,三次输注组中更多受试者达到至少5分改善(组间差异11.5%,后验概率98.4%,图2A)和11分改善(组间差异42.4%,后验概率≥99.9%,图2B),均优于安慰剂组。
相反,两次输注组受试者达到5分改善(组间差异54.6%,后验概率99.9%,图2A)和11分改善(MD:−43.1%,95%CrI:−69.8%至 −13.6%,PP=99.7%;图2B)的比例均低于安慰剂组。
总体评估:MDS-UPDRS总分的改善
在总分改善方面,三次输注组在第62周时有更多参与者达到至少12分改善(MD:22.0%,95%CrI:−21.0%至49.4%,PP=96.3%),在第88周改善更为显著(MD:48.4%,95%CrI:23.9%至74.0%,PP≥99.9%)。
相反,两次输注组在第62周(MD:−43.0%,95%CrI:−71.2%至 −8.3%,PP=99.1%)和第88周(MD−20.8%,95%CrI:−53.1%至14.1%,PP=87.8%)均劣于安慰剂组。
治疗安全性与免疫反应评估
安全性结果是本研究的亮点之一。整个研究期间:共报告10例轻微、短暂的治疗相关不良事件,无任何严重不良事件(SAEs)发生。三次输注组报告了个别不适症状(如全身不适、短暂性高血压)。两次输注组报告的症状均为自限性的全身症状(如疲劳、流感样症状),均自行缓解。
起初有三例疑似供者特异性抗体(DSA)的反应,经后续HLA分型确认均与治疗无关,其中一例实际来自安慰剂组。
结果表明,重复输注同种异体hMSCs安全且耐受性良好,未引发显著的免疫原性或任何致瘤性担忧。
综合讨论:疗效差异的解读与启示
主要疗效结果:三次输注组显著优于安慰剂
分析显示,主要疗效结果已达到。与安慰剂组相比,接受三次输注的治疗组在第62周时有更高比例的患者实现MDS-UPDRS-III评分≥5分(高出5%)和≥11分(高出13.3%)的改善,且该优势到第88周时进一步扩大(分别高出11.5%和42.4%),后验概率均高于91.5%,显示出强烈的统计学意义。
起效时间与作用机制推测
三次输注组起效迅速,首次输注后9周即观察到显著运动症状改善(降低12.9分),这表明同种异体hMSC可能在给药后通过快速调节免疫微环境发挥治疗作用。相比之下,两次输注组效果延迟且微弱,推测较晚输注时炎症环境已改变,可能导致细胞疗效降低。
两次输注组疗效欠佳的可能解释
该组疗效低于安慰剂的现象值得深入探讨,可能原因包括:
强大的安慰剂效应:安慰剂组显示了持续且显著的改善(改善14.6分),这可能掩盖了两次输注方案带来的微小获益。
输注时机与免疫环境:推测首次输注安慰剂时,患者处于更具反应性的炎症状态,而延迟输注活性细胞时,免疫环境可能已发生改变,导致细胞疗效降低。
批次间变异性:不同生产批次的MSCs在功能效价上可能存在差异,影响了治疗效果的一致性。
生活质量指标与多维评估的重要性
除了运动评分,PDQ-39和EQ-5D-5L等生活质量指标显示,治疗组在患者日常功能和幸福感方面优于安慰剂组,且改善持续更久。这凸显了运动评估(MDS-UPDRS-III)存在局限性,在PD临床试验中纳入患者报告的生活质量等多维终点至关重要。
结论
据我们所知,这是首个采用三次重复静脉注射剂量(每次10×10^6个异基因人间充质干细胞/千克)的随机、安慰剂对照试验。
该研究达到了其主要疗效终点:与安慰剂相比,三次注射剂量(每次10×10 6个异基因人间充质干细胞/千克)治疗有超过70%的可能性改善了轻度至中度帕金森病患者的运动评分。安慰剂组患者的运动评分显著改善,而两次输注组的改善程度则略逊一筹,这值得进一步研究和临床试验。
该治疗耐受性良好,所有报告的不良事件均为轻微且短暂的。未发现严重的治疗相关不良事件,也未报告免疫原性或致瘤性。这些结果支持了一种非侵入性、可扩展且符合伦理道德的帕金森病干细胞疗法的安全性和潜在疗效。
未来需要进行额外的功能效价测定,以确保异基因人间充质干细胞批次的一致性和可靠性。需要进一步进行大规模、多中心研究来证明同种异体hMSCs在减轻PD的运动和非运动症状方面的全部治疗潜力。
参考资料:
表1,表2详细结果可后台留言获取
[1]:https://movementdisorders.onlinelibrary.wiley.com/doi/10.1002/mds.28582
[2]:https://movementdisorders.onlinelibrary.wiley.com/doi/10.1002/mds.70028
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。
郑重声明:本文版权归原作者所有,转载文章仅为传播更多信息之目的,如作者信息标记有误,请第一时间联系我们修改或删除,多谢。



发表回复