引言: 2型糖尿病(T2D)是最常见的糖尿病类型,影响着全球6.28%的人口。几十年来,人们开发了多种疗法和药物来控制T2D,但它们远非长期解决方案。干细胞作为一种新型再生疗法展现出巨大的潜力,尤其是间充质干细胞(MSCs),它们具有高度多样化的再生和旁分泌能力及特性。这使得它们成为最常用的成体干细胞,也是治疗糖尿病的理想候选者。
干细胞治疗2型糖尿病安全有效被再次证明:262例患者血糖明显降低,胰岛素需求减少
近日,期刊杂志《Diabetes, Metabolic Syndrome and Obesity》发表了一篇“间充质干细胞治疗2型糖尿病的安全性和有效性——文献综述”的研究综述的文章,本综述旨在评估间充质干细胞(MSCs)治疗人类2型糖尿病(T2D)的安全性和有效性。结果表明:间充质干细胞治疗糖尿病安全有效。需要更大的样本量,并且试验还应研究分化 MSC 作为胰岛素分泌细胞的效果。

2型糖尿病(T2DM)是一种异质性疾病,其特点是脂质、碳水化合物和蛋白质代谢紊乱,并伴随胰岛素分泌受损、胰岛素抵抗或两者兼有。与1型糖尿病(也称胰岛素依赖型糖尿病)相比,T2DM在全球的患病率更高:2021年约有5.37亿患者,预计2030年将增至6.43亿人,2045年将达到7.83亿人。T2DM主要发生于50岁以上人群,但在20岁以下的成年人和儿童中也越来越常见。若控制不佳,T2DM可导致长期并发症,如缺血性心肌梗死、中风、慢性肾病及糖尿病视网膜病变。
2型糖尿病的常规疗法包括改变生活方式和饮食习惯以控制体重和热量摄入,以及口服降糖药物,例如利拉鲁肽(Victoza)、索玛鲁肽(Ozempic)和度拉糖肽(Trulicity),最终可能需要每日注射胰岛素。对于晚期2型糖尿病,胰腺移植仍然是主要的治疗选择,但费用昂贵且复发风险高。2型糖尿病的常规治疗方法存在诸多局限性。化疗药物会带来多种副作用,包括肝毒性、低血糖、胃肠道紊乱、呼吸道感染等。此外,这些治疗并不能减缓胰岛β细胞功能的衰退,而只是缓解疾病症状(图1)。
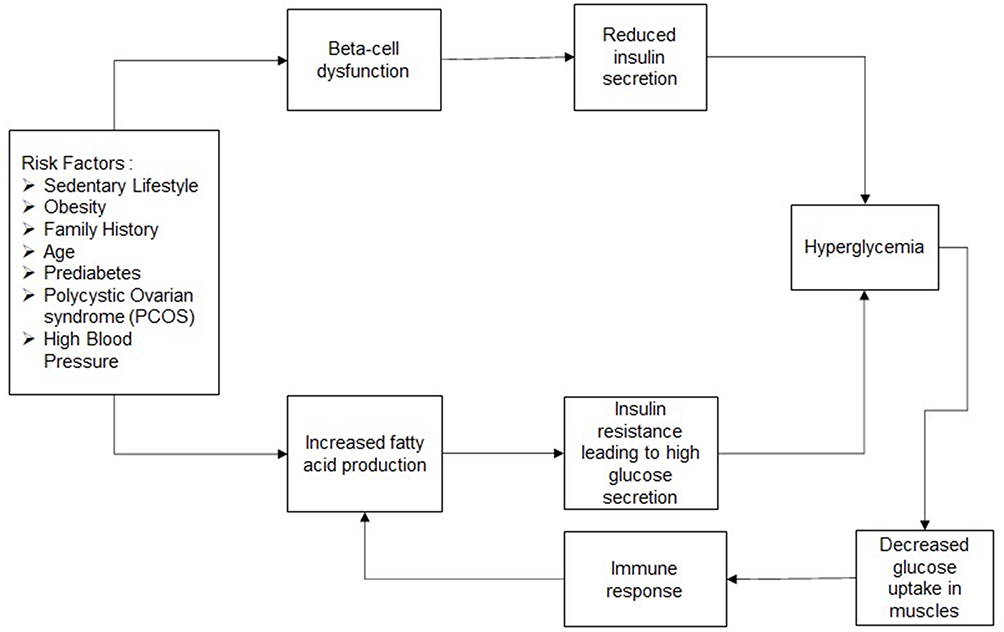
图1流程图 – 2型糖尿病:如上所述,2型糖尿病是由多种风险因素引起的。这些因素会逐渐导致β细胞功能障碍。β细胞功能低下或功能障碍会减少胰腺胰岛素的分泌,进而导致高血糖。这些风险因素还会导致肝脏脂肪酸生成增加,从而导致肝脏分泌大量葡萄糖。葡萄糖分泌增加会降低胰岛素的功能,导致胰岛素抵抗。高血糖会导致肌肉对葡萄糖的吸收减少,并引发免疫反应。这会进一步损害肝脏并加剧胰岛素抵抗。
传统治疗存在多重局限性:当生活方式干预或化疗药物无法控制血糖水平时,需要注射胰岛素,但胰岛素注射是一种侵入性操作,且存在其他风险。依从性差可能导致不良事件,例如脂肪增生、感染、注射部位皮肤过敏以及产生针对外源性胰岛素的抗体。因此,替代疗法对于2型糖尿病的治疗至关重要。
干细胞疗法为T2DM治疗带来了新希望。干细胞具有自我更新、再生和分泌关键调节因子的能力,已在帕金森病、多发性硬化、多发性骨髓瘤等疾病的临床试验中进行探索。用于T2DM研究的主要干细胞类型包括:
-
间充质干细胞(MSCs)
-
造血干细胞
-
诱导多能干细胞(iPSCs)
其中,MSCs在T2DM临床试验中应用最广,因为可从自体或异体骨髓、脂肪组织和血液等多种来源分离¹⁵。MSCs具备多向分化潜能且免疫原性低,表达低水平MHC-I、无MHC-II,不会触发T细胞增殖反应。
为克服当前治疗策略的不足,研究人员正在开发基于MSCs、iPSCs及造血干细胞的干细胞输注疗法。本研究将聚焦于使用间充质干细胞的临床试验,评估其在晚期T2DM患者中的安全性与疗效。
方法
搜索资源和策略:数据来源于PubMed和clinicaltrials.gov数据库,检索词包括“2型糖尿病”、“干细胞疗法”、“糖尿病”、“间充质干细胞疗法”、“骨髓间充质干细胞”、“2型糖尿病”、“T2DM”、“BM-HSC”、“脐带间充质干细胞”,检索范围限定为2011年至2021年间完成的临床试验。检索策略遵循系统评价和荟萃分析报告规范(PRISMA)指南。语言限定为英语。纳入了干预性研究和观察性研究。荟萃分析排除了评估方法信息不足、合并其他慢性疾病以及样本量过小(<10例患者)的临床试验。
数据提取:数据提取按照Cochrane系统评价指南进行。筛选和检索基于试验类型(干预性或观察性)、参与者(年龄、样本量、2型糖尿病病程)、2型糖尿病治疗方法以及疗效指标,例如糖化血红蛋白(HbA1c)、C肽和空腹血糖(FPG)水平。
结果
共收集到70项试验;剔除重复记录后,剩余58项。在这58项临床试验中,仅纳入6项研究(T1、T2、T3、T4、T5、T6)、262例糖尿病患者(表1)。其余研究存在以下问题:需要更全面的结果;治疗评估方法信息不足;旨在报告与2型糖尿病相关的长期合并症的治疗而非疾病本身;非随机对照试验;以及受试者合并其他疾病。纳入荟萃分析的研究均采用自体间充质干细胞注射,无论其来源如何。
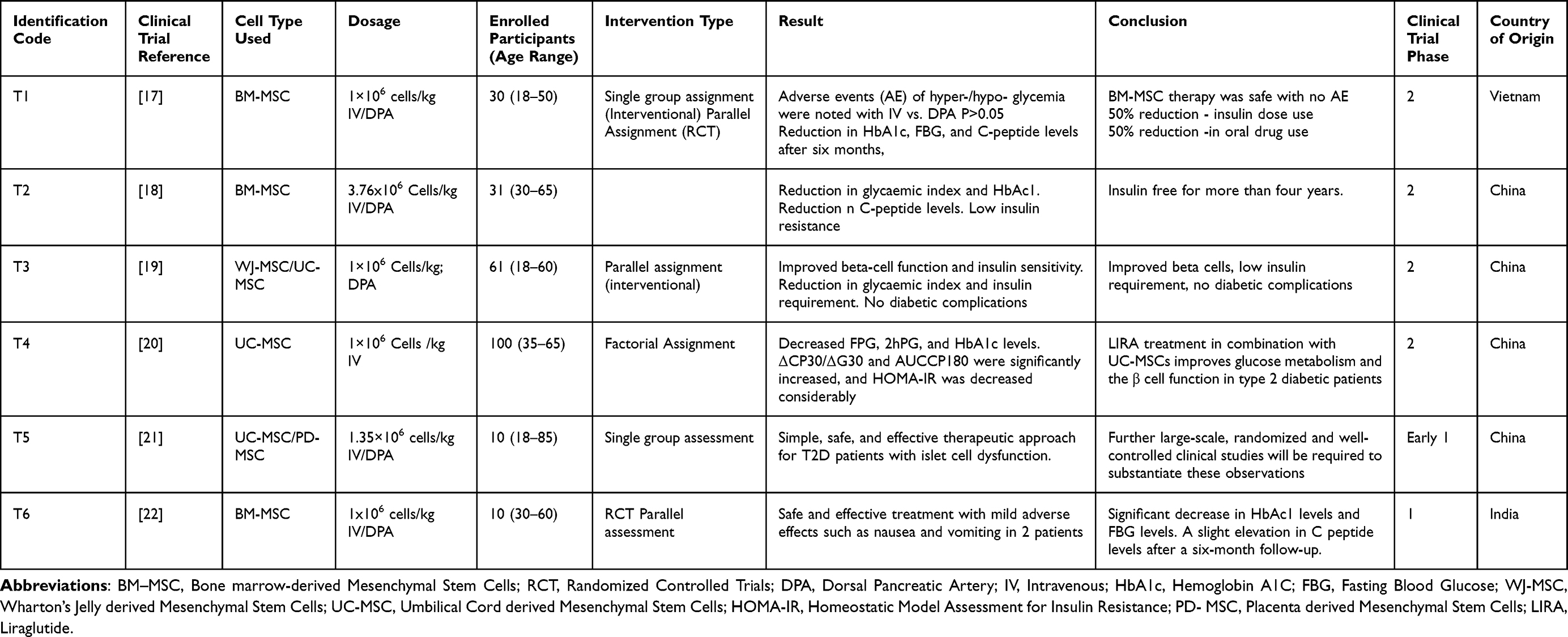
表1临床试验:基于间充质干细胞的2型糖尿病疗法
总体预后与血糖控制得到根本改善
间充质干细胞治疗能显著改善2型糖尿病患者的整体预后。多项临床试验表明,治疗能有效降低胰岛素抵抗和患者对外源性胰岛素的依赖,且这一疗效与患者的病程长短及MSCs的组织来源无关(图2)。关键指标如糖化血红蛋白(HbA1c) 和空腹血糖(FBG) 均出现显著下降,其中空腹血糖可恢复至正常范围,这提示患者的长期血糖控制水平和肝脏糖代谢功能得到了根本性改善。
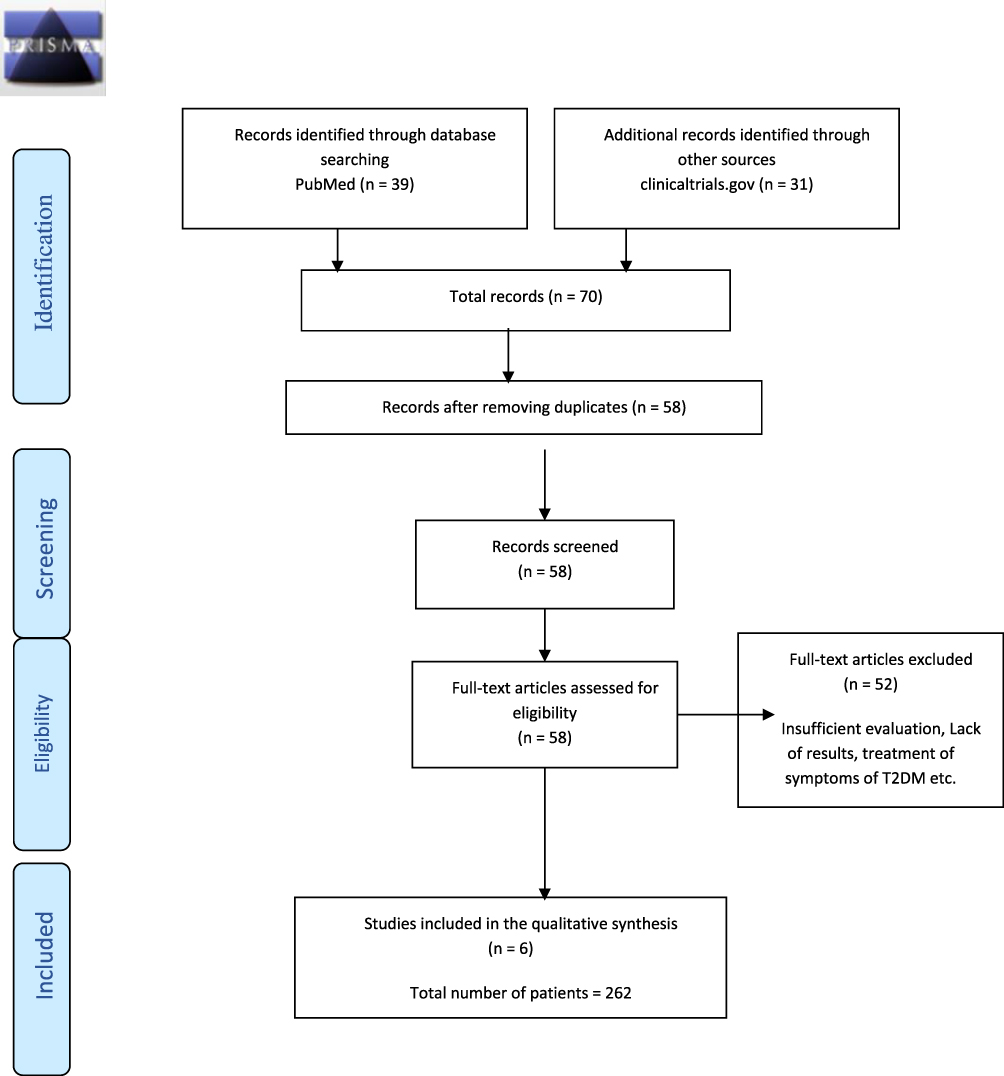
图2研究分析的 Prisma 图。该图描绘了纳入本文的研究的纳入和排除标准。
有效缓解胰岛素抵抗
治疗在缓解胰岛素抵抗方面效果突出。注射MSCs后,患者的胰岛素依赖性可显著降低长达12个月。通过稳态模型评估(HOMA)显示,胰岛素抵抗指数(HOMA-IR) 得以降低,这标志着机体对自身胰岛素的利用效率提升。尽管有个别研究未报告此指标的显著变化,但所有研究均通过患者所需胰岛素剂量的减少,共同印证了MSCs在改善胰岛素抵抗方面的积极影响(图3)。
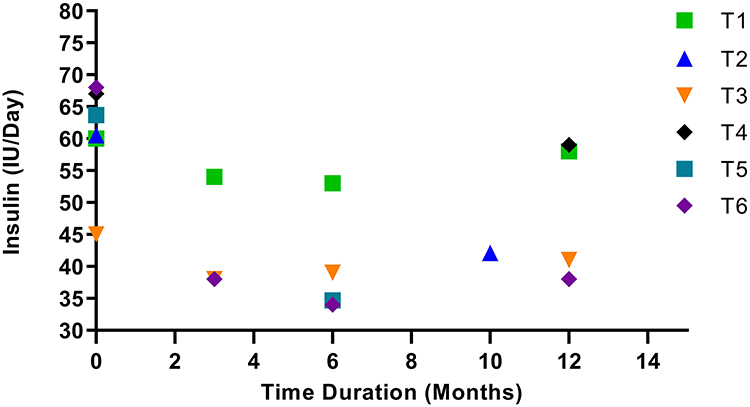
图3显示了MSC治疗前后胰岛素需求量的变化。各试验的随访时间不同。T1、T3和T6组在3个月和6个月的随访期内胰岛素需求量均有所下降,但在12个月的随访期内胰岛素需求量持续上升。T5组在6个月的随访期内胰岛素需求量下降了45%,但该研究未进行后续随访。T4组在12个月的随访期内胰岛素需求量下降了22%。T2组在10个月的随访期内胰岛素需求量下降了30%,之后该研究未进行后续随访。
促进胰岛β细胞功能恢复
治疗对代表胰岛β细胞功能的C肽水平 产生了积极的调节作用。研究结果显示,C肽水平呈现两种积极的变化趋势:一部分患者的C肽水平升高,直接反映了β细胞分泌胰岛素能力的恢复;另一部分患者则表现为C肽降至正常范围,这在此前C肽水平过高的患者中,意味着其伴随胰岛素抵抗的“高胰岛素血症”得到纠正,胰岛功能趋于正常。多数研究中,C肽水平在治疗后6个月达到峰值并能在12个月内保持稳定(图4)。
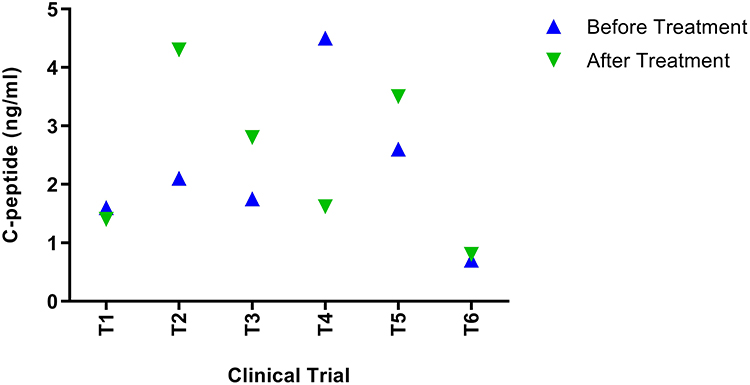
图4显示了MSC移植后C肽水平的变化。T1和T4组的C肽水平分别下降了12%和64%。T2、T3和T5组的C肽水平分别上升了62%、40%和34%。T6组治疗后C肽水平上升了10%。
实现长期稳定的血糖控制
MSCs治疗在长期血糖控制上展现出强大潜力。作为衡量过去2-3个月平均血糖水平的“金标准”,糖化血红蛋白(HbA1c) 在所有试验中均被观察到显著下降,且在长达12个月的随访期内效果持续增强。这一趋势证明MSCs治疗带来的不是短暂的血糖波动,而是持续、稳定的代谢调控。尽管在合并肾病的患者中此效果可能受限,但总体而言,HbA1c的持续改善强有力地证明了MSCs治疗能为2型糖尿病患者带来长期健康收益(图5)。
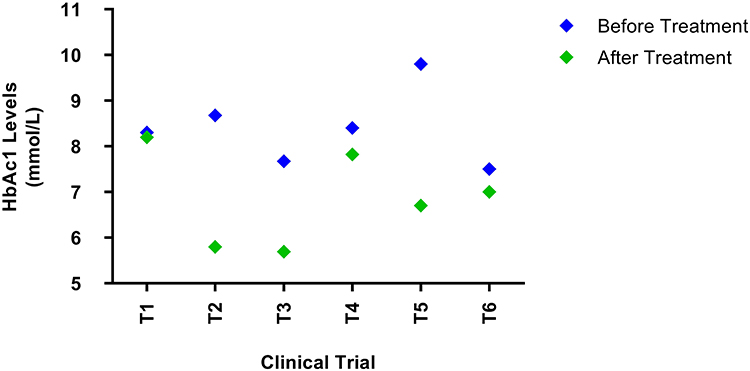
图5显示了MSC治疗前后HbA1c水平的变化。所有试验中HbA1c水平均显著下降。随访后,T1、T2、T3、T4、T5和T6组的HbA1c水平分别降至1.2%、32%、26%、7.1%、31%和6%。
不良事件
除两项研究T1和T6(表1)观察到部分患者出现恶心和呕吐外,所有研究均未观察到严重不良事件。其中一项研究T1还观察到低血糖。所有研究均认为该治疗方法有效且安全。
证实疗法安全有效,展现长期潜力
综合分析表明,间充质干细胞治疗2型糖尿病具有高度的安全性和明确的有效性。在涵盖262名患者的临床试验中,该疗法未报告严重不良反应,仅出现轻微不适,其安全性得益于MSCs低免疫原性及使用自体细胞来源。
在疗效上,在 12 个月的随访期内,间充质干细胞 (MSC) 治疗降低了患者的降糖药物剂量。有效治疗剂量范围为1×10⁶个细胞/kg 至 3.7×10⁶个细胞/kg。治疗后,糖化血红蛋白 (HbA1c) 水平平均降低了 32%,空腹血糖水平平均降低了45%。在两项试验中,C肽水平平均降低了38%,而在四项试验中,C肽水平平均升高了36%。所有试验均未观察到严重不良事件。这证明单次治疗即可在长达一年的时间里稳定控制血糖,成为一种极具潜力的长期解决方案。
明确治疗优势与未来研究方向
讨论结果进一步明确了该疗法的实用优势:不同的细胞输注途径(静脉或胰背动脉)对疗效无显著影响,这增加了临床操作的灵活性;同时,与传统胰腺移植相比,它虽费用相当但仅需单次给药,侵袭性更小。然而,研究也指出当前局限,如因严格的入组标准导致样本量有限。因此,未来需要通过纳入更多患者、延长随访时间、并针对不同病程患者进行研究,以进一步精确评估其疗效,推动该疗法向标准化临床应用迈进。
结论
总之,研究表明间充质干细胞(MSCs)治疗有效且经济。应在2型糖尿病早期患者中研究这种治疗模式的影响,以了解其是否能带来长期疗效。此外,由于需要统一的样本人群以及纳入和排除标准,每项研究的意义有所降低。因此,需要更大、更统一的样本量和更连续的随访期。这些研究应测量胰岛素抵抗、胰岛素依赖性、C肽值和糖化血红蛋白(HbA1c)值。
参考资料:Mathur A, Taurin S, Alshammary S. The Safety and Efficacy of Mesenchymal Stem Cells in the Treatment of Type 2 Diabetes- A Literature Review. Diabetes Metab Syndr Obes. 2023;16:769-777
https://doi.org/10.2147/DMSO.S392161
郑重声明:本文版权归原作者所有,转载文章仅为传播更多信息之目的,如作者信息标记有误,请第一时间联系我们修改或删除,多谢。



发表回复