帕金森病(Parkinson’s disease, PD)是仅次于阿尔茨海默病的第二大常见神经退行性疾病,其核心病理特征为中脑黑质区多巴胺能神经元的进行性丧失,伴随α-突触核蛋白异常聚集。临床上表现为运动迟缓、静止性震颤、肌强直等运动症状,以及认知障碍、抑郁等非运动症状,严重影响患者生活质量。
当前主流治疗手段包括左旋多巴等多巴胺替代药物、外科手术及脑深部电刺激,虽能在一定程度上缓解症状,却无法阻断病程进展。长期用药还常诱发运动波动、异动症及精神副作用等并发症。在此背景下,以修复神经损伤为目标的细胞疗法逐渐成为研究热点。同时,生活方式干预,尤其是饮食调控,在PD管理中的作用日益受到重视。值得注意的是,特定饮食模式已被证实可影响干细胞更新与再生能力——这一现象在肿瘤学领域已有探讨。生酮饮食联合干细胞治疗帕金森病,即通过高脂肪、极低碳水化合物的代谢干预方案与多巴胺能神经元干细胞疗法相结合,或可为PD提供一种兼顾症状控制与病程干预的综合治疗策略。
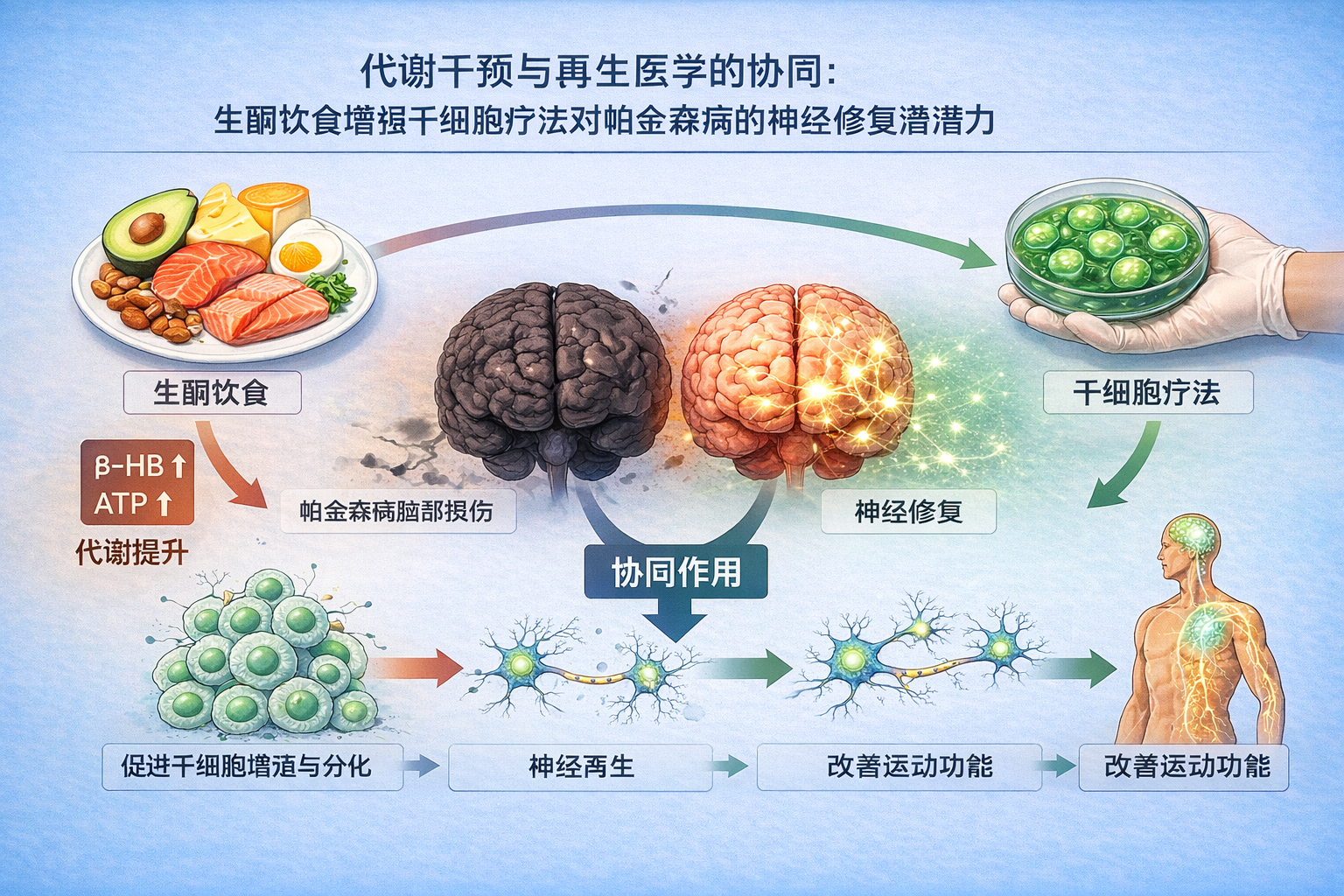
协同与修复:生酮饮食联合干细胞治疗帕金森病的理论探索
协同与修复:生酮饮食联合干细胞治疗帕金森病的理论探索
PD的发病机制复杂,涉及线粒体功能障碍、蛋白稳态失衡、神经炎症等多重因素。针对这些病理环节,联合应用生酮饮食与干细胞疗法,有望在现有治疗基础上实现协同增效。为系统探讨这一策略的潜力,我们于2026年2月9日在《Cureus医学科学杂志》发表综述《生酮饮食与干细胞疗法在帕金森病中的潜在协同作用》[1],旨在剖析二者机制、探讨联合应用能否减轻传统治疗副作用、提升疗效,并提出未来研究方向,包括高效干细胞递送系统的研发,以及生酮饮食在神经退行性疾病中长期应用的可行性与挑战。

一、代谢重塑与神经保护:生酮饮食干预PD的理论依据
生酮饮食改善PD症状的首要机制在于其对脑能量代谢的重塑与线粒体功能的支持。PD患者脑中普遍存在葡萄糖利用障碍及线粒体呼吸链复合物I功能缺陷,诱发神经元能量危机与氧化损伤。生酮饮食通过严格限制碳水化合物摄入,诱导机体进入以脂肪供能为主的“酮症”状态,肝脏生成酮体(如β-羟基丁酸),可作为高效、稳定的替代能源,绕过受损糖代谢通路,直接为神经元供能。
研究表明,酮体不仅能提升线粒体生物合成与氧化磷酸化效率,还可减少线粒体源性活性氧生成,从而保护多巴胺能神经元,改善运动及非运动症状。此外,酮体本身具备抗炎、抗氧化、调节神经递质及增强细胞应激耐受等多重作用;生酮饮食还可促进自噬、改善胰岛素敏感性、降低兴奋性毒性,全面干预PD的多重病理环节。
临床观察亦显示,生酮饮食有助于稳定血糖、改善体成分与代谢指标,这些整体代谢状态的优化与患者生活质量提升密切相关。因此,从代谢干预角度出发,生酮饮食被视为一种具有内在病理调节潜力的非药物辅助策略。

二、协同增效的理论基础:生酮饮食优化干细胞移植微环境
生酮饮食与干细胞疗法联合应用的核心逻辑在于:生酮饮食不仅优化大脑能量供应、改善PD相关代谢缺陷,还能通过酮体系统性减轻氧化应激与神经炎症。这种整体内环境的改善,有望增强多种成体干细胞(如神经干细胞、间充质干细胞)的自我更新与再生能力。在干细胞移植前后配合生酮饮食,可为移植细胞营造一个更有利于存活、整合与功能发挥的微环境,从而实现协同增强效应。
生酮饮食影响干细胞功能的主要机制包括:
- 能量与代谢调节:酮体作为高效能量底物被干细胞利用,并通过影响p53等关键蛋白的乙酰化修饰,维持干细胞稳态;
- 激活保护性信号通路:生酮饮食可上调转录因子NRF2,抑制NF-κB等促炎通路,调控并增强干细胞的再生潜力。
然而,将该联合策略推向临床仍面临三大挑战:
- 证据基础薄弱(现有支持多来自临床前研究或小规模观察,缺乏高质量临床试验);
- 生酮饮食实施困难(老年患者依从性差、营养风险、缺乏标准化方案);
- 干细胞技术瓶颈(细胞来源、存活率、免疫排斥、致瘤风险及功能整合等)。
因此,尽管理论前景广阔,仍需大量严谨研究以克服转化障碍。
三、研究方法与文献基础
本研究采用非系统性文献综述方法,通过检索Google Scholar、PubMed/MEDLINE、PubMed Central等数据库,使用“帕金森病”、“生酮饮食”、“干细胞疗法”、“线粒体功能障碍”等关键词组合,收集已发表文献。同时辅以引证检索,追踪关键文献的参考文献,以构建广泛的文献基础。
证据筛选以临床前研究(体外及动物模型)、临床研究及综述文章为主,优先纳入与综述目标高度相关、能提供清晰机制解释或临床见解的文献。由于本文为叙述性综述,未遵循系统评价的正式流程(如预设纳入标准、PRISMA流程图或偏倚风险评估),而是按主题对文献进行定性综合,以支撑各部分的论述逻辑。
四、生酮饮食的核心机制与应用拓展
经典生酮饮食的宏量营养素构成约为55–60%脂肪、30–35%蛋白质、5–10%碳水化合物。其核心在于严格限制碳水化合物摄入,显著降低胰岛素分泌,诱导机体进入“营养性酮症”状态,肝脏将游离脂肪酸代谢生成酮体,作为大脑等重要器官的替代能源。
生酮饮食最初用于治疗儿童难治性癫痫,后逐步拓展至代谢性酶缺乏、婴儿痉挛症、Rett综合征、结节性硬化症等疾病。近年来,其在神经退行性疾病(包括PD)中的应用潜力备受关注。
在PD背景下,生酮饮食的可能机制包括:
- 提供替代能量,改善脑代谢;
- 增强线粒体复合物I活性,促进线粒体生物合成(如激活PGC-1α通路),改善线粒体动力学;
- 减轻氧化应激,保护多巴胺能神经元;
- 抗炎与神经保护,调节小胶质细胞活性,抑制促炎信号通路。
临床前研究进一步揭示:在MPTP诱导的PD小鼠模型中,酮体显示出神经保护作用;长期生酮饮食可诱导慢性酮症,促进大脑代谢适应,并改变皮层细胞(星形胶质细胞、神经元、小胶质细胞)的蛋白质组与代谢谱,优化能量底物输送与利用。这些发现表明,生酮饮食通过多靶点代谢干预,具备调控神经疾病进程的潜力,但患者依从性差仍是主要临床挑战。
五、干细胞疗法:从替代修复到精准重建
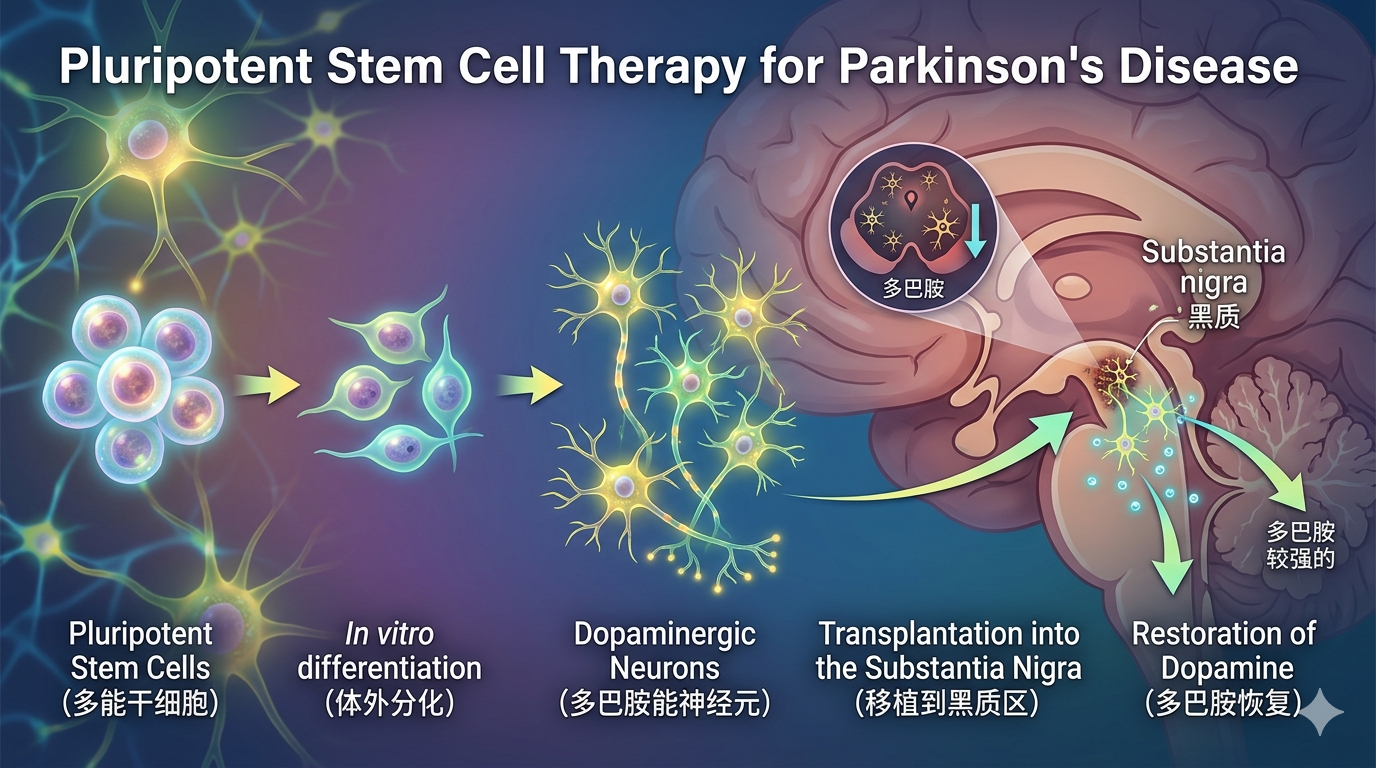
干细胞疗法治疗PD的基本原理在于:通过移植多巴胺能神经元前体细胞,直接补充和修复退化丢失的神经元网络,尤其是黑质至纹状体通路。其核心优势在于“治本”型再生策略,有望实现更精准、更生理性的神经环路重建,提供更持久稳定的治疗效果。
主要干细胞类型包括:
- 胚胎干细胞(ESCs):来源于早期胚胎,具有强大分化潜能,可定向分化为表达LMX1A、FOXA2等黑质多巴胺能神经元标志物的细胞。但存在伦理争议、免疫排斥及来源有限等问题。
- 诱导多能干细胞(iPSCs):通过对患者自体细胞重编程获得,可构建个体化移植产品,避免免疫排斥,伦理问题较少,是目前更具临床转化前景的细胞来源。
干细胞疗法的必要性源于现有药物治疗的严重局限:仅为症状缓解,无法阻断病程;长期使用左旋多巴可致运动波动、异动症及精神副作用;血脑屏障功能障碍影响药物精准递送。干细胞疗法则有望从根本上修复神经环路,实现功能重建。
然而,其临床转化仍面临多重挑战:
- 科学与技术挑战:确保干细胞高效分化为功能成熟的黑质多巴胺能神经元亚型;移植后细胞长期存活、整合、建立功能性连接,避免异常增殖;
- 临床与转化挑战:建立标准化生产与质控流程;验证长期安全性(免疫反应、致瘤性)与有效性;确定最佳移植参数;
- 疾病复杂性挑战:PD常伴认知障碍,干细胞疗法需兼顾运动与认知环路的恢复,增加治疗目标复杂性。
六、讨论:联合策略的理论框架与转化前景
本综述探讨了生酮饮食联合干细胞疗法对PD病程、症状及病理机制的影响。现有药物治疗虽可缓解运动症状,但伴随神经精神副作用、运动并发症等局限,且无法逆转病情。因此,探索能根本干预疾病进程的新策略至关重要。
在临床前模型中,干细胞移植已被证实可改善PD动物运动功能,延长存活期。同时,生酮饮食通过提供替代能源、增强抗氧化防御、抑制神经炎症、改善线粒体功能,为内源及移植神经元创造有利微环境。
本研究提出一个前瞻性理论框架:将生酮饮食作为干细胞疗法的辅助手段,可能产生协同增效。一方面,生酮饮食通过改善整体代谢、降低氧化应激与炎症,优化干细胞移植前体内环境,促进移植后细胞存活与整合;另一方面,借鉴肠道等组织的研究发现,特定饮食模式可显著影响干细胞自我更新与再生能力,提示通过饮食代谢干预调节神经干细胞命运是可行的。
结合“肠-脑轴”在PD中的作用,这种饮食与再生医学的联合策略,理论上可从能量代谢、氧化应激、炎症、肠道微环境等多个层面共同调节疾病进程,为解决PD根本病理问题提供创新综合治疗思路。然而,该联合方案的有效性与安全性仍需未来深入研究与临床试验加以验证。
七、生酮饮食联合干细胞治疗帕金森病的局限性
本综述存在以下局限性:
- 证据来源局限:支持生酮饮食与干细胞疗法治疗PD的大部分证据来自体外实验和动物模型研究,未能完全涵盖人类PD的复杂性、异质性与慢性进展特征;
- 缺乏联合治疗临床试验:目前尚无评估生酮饮食联合干细胞疗法治疗PD的临床试验,任何协同获益均属假设性推论;
- 干细胞疗法自身局限:存在免疫相容性、移植细胞长期存活率、致瘤风险、患者病程差异及移植神经元异质性等转化障碍;
- 生酮饮食实施困难:老年患者依从性差,存在微量营养素缺乏等潜在风险。
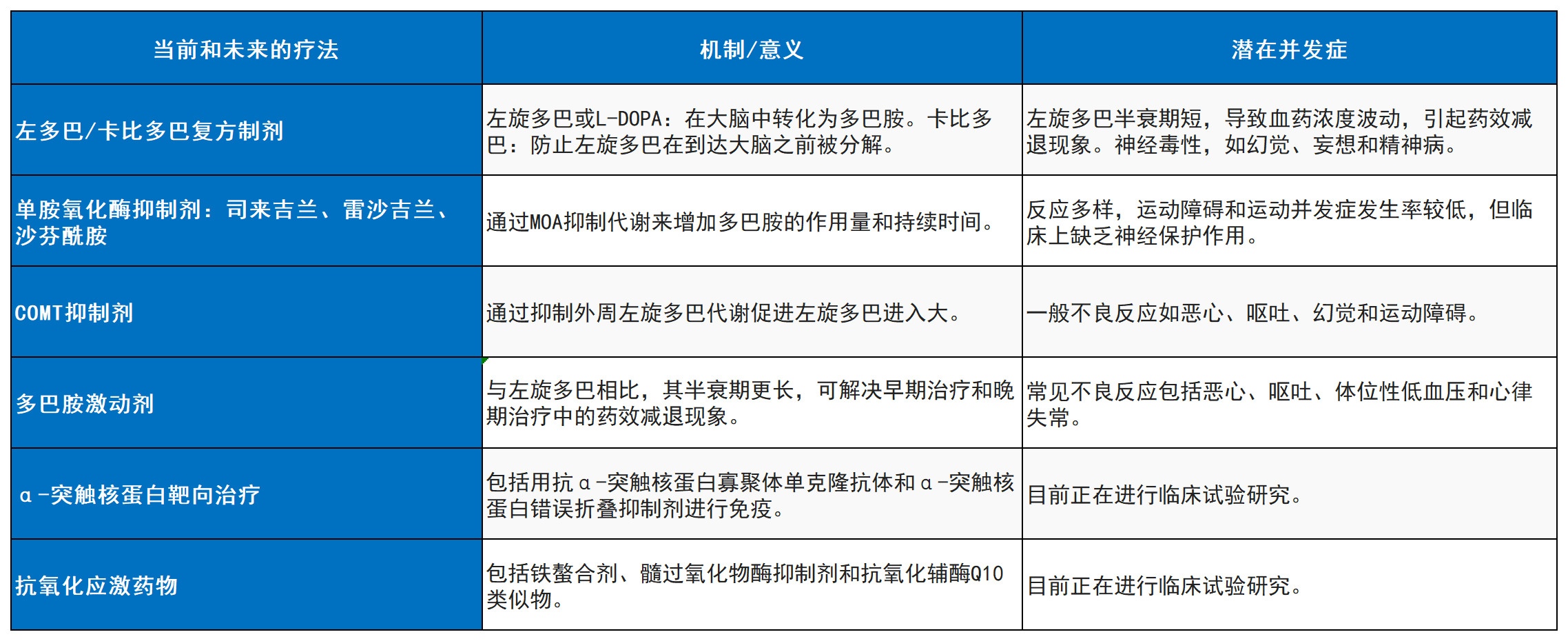
因此,在将生酮饮食与干细胞疗法联合应用于PD疾病干预之前,需进行严格的临床验证与精心设计的临床试验。表1归纳了当前PD的主要治疗方法。
八、结论
本综述探讨了干细胞疗法与生酮饮食在PD治疗中的潜在协同作用。尽管传统疗法有效,但其副作用显著,尤其对老年患者影响较大。动物模型研究表明,干细胞疗法可显著改善PD病情,生酮饮食亦能有效控制症状。二者联合应用,有望减轻现有疗法副作用,提升治疗效果。
未来需进一步研发高效的干细胞递送系统,并深入研究生酮饮食与干细胞疗法的相互影响。同时,开展PD患者长期随访研究,将有助于深化对PD发病机制的理解,为联合治疗策略的优化提供依据。
参考资料:[1] Sindurakar P, Gorantla VR, Ponnoth D.生酮饮食和干细胞疗法在帕金森病中的潜在协同作用:叙述性综述。*Cureus*, 2026, 18(2): e103304。DOI: 10.7759/cureus.103304。
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议。杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系。
郑重声明:本文版权归原作者所有,转载文章仅为传播更多信息之目的,如作者信息标记有误,请第一时间联系我们修改或删除,多谢。



发表回复