
2026年干细胞治疗应用展望:干细胞如何改变当今医学
一、干细胞疗法的主要优势与医学价值
干细胞治疗之所以被视为革命性医疗突破,源于其以下几大核心优势:
- 自我更新与多向分化潜能:可在体内外持续增殖并分化为所需的功能细胞,为组织修复提供“细胞源泉”。
- 旁分泌效应与免疫调节:通过释放生长因子、细胞因子和外泌体等,调节局部微环境,促进内源性修复。
- 来源多样性与个性化潜力:包括胚胎干细胞、成体干细胞、诱导多能干细胞(iPSC)等,尤其iPSC技术可实现患者特异性治疗,避免免疫排斥。
- 技术融合性强:可与基因编辑、3D生物打印、类器官培养等技术结合,拓展应用边界。
二、干细胞在医学中的核心应用领域
过去几十年,干细胞已从实验室研究工具演化为具有六大主流应用方向的医疗技术平台,预计到2026年干细胞治疗应用展望方向将进一步深化与扩展。
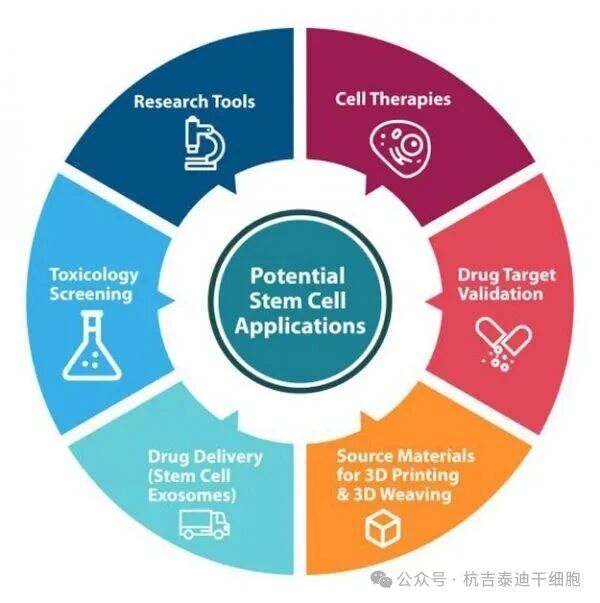
1.作为研究工具:揭示生命机制与疾病本质
干细胞是实验室中不可或缺的研究工具,可用于理解基础生物学过程、疾病机制和药物研发。它们为研究细胞分化、发育和疾病建模提供了一个独特的平台。研究人员可以操控干细胞分化成各种细胞类型,从而深入了解组织发育和发病机制。此外,干细胞还可以进行基因改造以构建疾病模型,进而研究疾病进展和筛选潜在的治疗方法。
2. 细胞治疗:再生医学的核心引擎
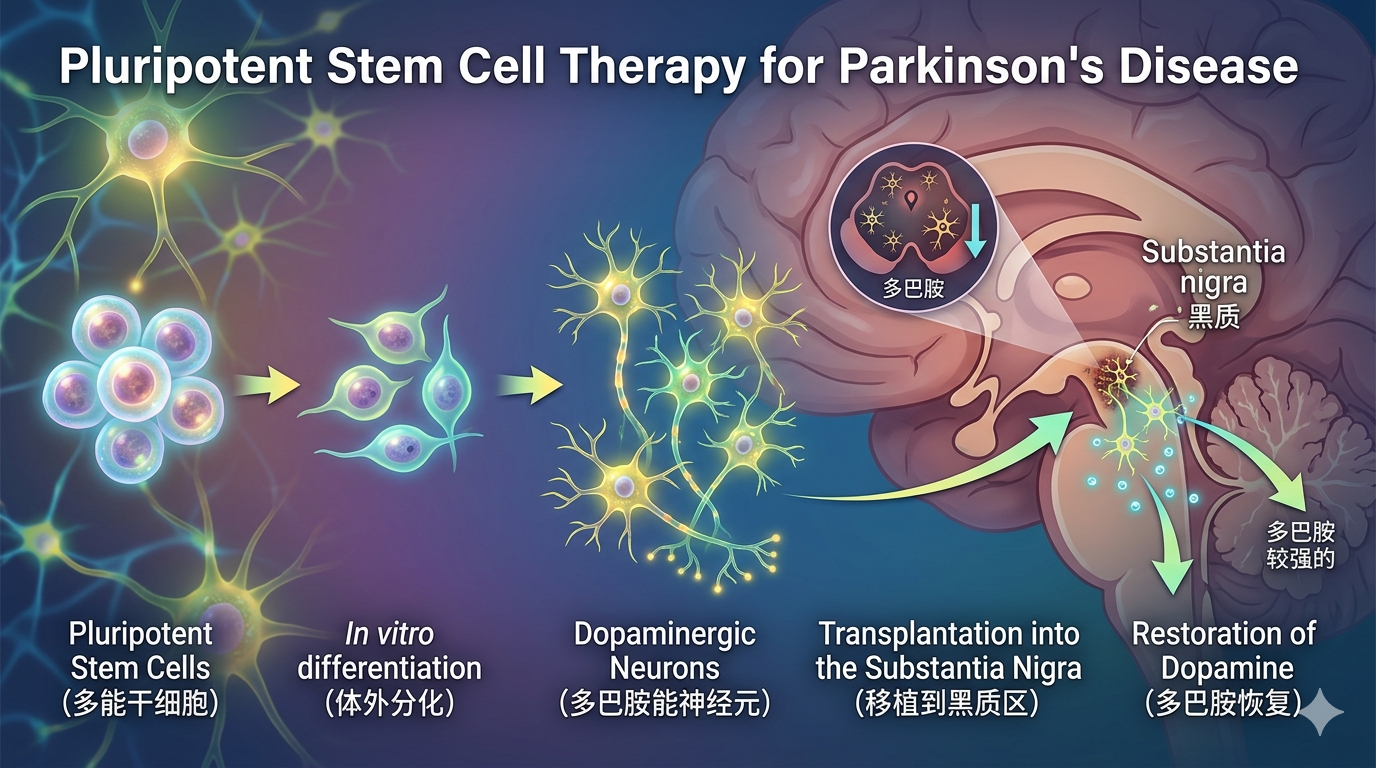
- 神经退行性疾病:多能干细胞分化的多巴胺能神经元用于帕金森病治疗已进入临床试验。
- 心血管修复:利用干细胞或由其分化的心肌前体细胞修复梗死心肌,改善心功能。
- 代谢性疾病:胰岛β细胞移植治疗Ⅰ型糖尿病的研究不断取得突破。
- 骨科与运动医学:间充质干细胞注射促进软骨、骨骼与肌腱修复,已逐步应用于骨关节炎、运动损伤等。
- 自身免疫与炎症性疾病:基于干细胞的免疫调节疗法为红斑狼疮、多发性硬化等提供新思路。
3. 组织工程与3D生物制造:打印生命的可能性
干细胞作为“活墨水”,在3D生物打印与编织技术中扮演关键角色:
- 器官芯片与类器官:用于药物筛选、疾病建模和毒性测试,减少动物实验依赖。
- 个性化植入物:结合患者影像数据,打印具有生物活性的骨、软骨甚至皮肤等复合移植物。
- 复杂器官再造探索:尽管全功能器官打印仍面临血管化等挑战,但肾单位、肝小叶等微型功能单元已成功构建。
4. 药物靶点验证与个性化药敏测试
组织特异性干细胞衍生的细胞是验证药物靶点和评估药物疗效的宝贵工具。通过将干细胞分化为模拟特定组织或器官的细胞,研究人员能在相关的生理环境中筛选潜在治疗化合物。这种方法提高了临床前药物测试的预测准确性,有助于识别有前景的候选药物进行进一步开发。基于干细胞的检测方法可阐明药物作用机制、识别脱靶效应,并加速药物发现进程。
5. 智能药物递送系统
- 肿瘤靶向治疗:装载抗癌药物的间充质干细胞可趋向肿瘤微环境,实现局部缓释。
- 神经修复:干细胞外泌体携带神经营养因子,穿透血脑屏障,促进神经再生。
- 抗纤维化与抗炎治疗:通过工程化改造,增强干细胞递送系统的精准性与效率。
6. 毒理学与新药安全评价
干细胞衍生的肝细胞、心肌细胞和神经元等已用于构建体外毒理测试平台,可更准确地预测药物肝毒性、心脏毒性及神经毒性,符合FDA等机构推行的“动物试验替代”与“微生理系统”战略。
三、2026年展望:突破、融合与挑战
到2026年,干细胞医学预计将在以下方面实现显著进展:
- 临床转化加速:更多干细胞产品获批上市,适应症从罕见病向常见病拓展。
- 制造工艺标准化与自动化:封闭式、自动化的干细胞扩增与分化系统将降低成本、提高质量可控性。
- 基因编辑与干细胞结合常态化:纠正患者干细胞致病突变后回输,用于治疗遗传性血液病、视网膜病变等。
- AI赋能干细胞医学:人工智能用于干细胞质量预测、分化路径优化、打印结构设计及治疗效果评估。
- 类器官与数字孪生系统:患者特异性类器官与个体生理数字模型结合,实现治疗方案的动态模拟与优化。
然而,挑战依然存在:
- 肿瘤形成与异质性风险:需进一步提高干细胞纯度与安全性。
- 免疫排斥与长期存活:即便使用iPSC,表观遗传记忆与突变积累仍需关注。
- 规模化与成本控制:制造工艺、质量检测与冷链物流成本仍是普及瓶颈。
- 伦理与监管框架:特别是涉及胚胎干细胞、基因编辑及脑类器官等领域,需全球协作建立科学合理的指南。
四、结语
干细胞不仅是一种治疗手段,更是一个贯穿基础研究、药物开发、临床治疗与健康管理的平台型技术。到2026年,随着跨学科协作的深入与技术瓶颈的逐步突破,干细胞有望真正实现从“修复组织”到“再造生命”的跨越,推动医学进入个性化、再生化和精准化的新时代。
我们正站在一个医学范式转变的门槛上——干细胞,这枚蕴藏在生命深处的种子,即将在科学的灌溉下,成长为一片改变人类健康的森林。
主要参考资料:bioinformant
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。
郑重声明:本文版权归原作者所有,转载文章仅为传播更多信息之目的,如作者信息标记有误,请第一时间联系我们修改或删除,多谢。



发表回复