帕金森病(PD)是一种以中脑黑质多巴胺能神经元进行性丢失为核心病理特征的神经退行性疾病。其临床表现不仅包括运动迟缓、肌强直等典型运动症状,还常伴有多种非运动症状(Non-Motor Symptoms, NMS),如抑郁、焦虑、认知障碍、嗅觉减退及睡眠障碍等。值得注意的是,许多NMS可在运动症状出现前数年甚至数十年出现,构成PD的运动前症状(premotor symptoms),严重影响患者生活质量与疾病预后。目前针对PD-NMS的药物治疗常伴随副作用或疗效局限。因此,探索能够间充质干细胞治疗帕金森病的新疗法势在必行。
间充质干细胞治疗帕金森病运动前症状的研究进展
近年来,以间充质干细胞(Mesenchymal Stem/Stromal Cells, MSCs) 为代表的生物疗法,凭借其神经保护、免疫调节及潜在神经修复功能,为PD-NMS的治疗带来了新希望。本文旨在综述间充质干细胞生物疗法改善帕金森病运动前症状的最新研究进展、潜在机制及临床应用前景。

帕金森病相关非运动症状(PD-NMS)、症状缓解及药物治疗
运动功能改善的治疗效果与维持大脑特定区域乙酰胆碱/多巴胺相对平衡的保护作用有关。除了单独使用口服左旋多巴药物或手术深部脑刺激来解决运动波动问题外,帕金森病非运动症状(PD-NMS)的发病率/患病率也呈现上升趋势。本文回顾了PD-NMS的治疗方法,旨在了解其现状,并尝试通过包括干细胞和益生菌植入在内的新型生物疗法来改善症状缓解(表1 )。
| 症状 | 临床干预 | 潜在生物疗法 | 其他建议 | ||
|---|---|---|---|---|---|
| 风险 | 配送路径 | ||||
| 焦虑 | 苯二氮卓类药物(地西泮、劳拉西泮) | 这会导致慢性压力,进而加剧神经阻滞剂症状。 | – | – | 进一步调节肠脑轴(肠道菌群中引入植物乳杆菌PS128) |
| 认知障碍 | 多奈哌齐、加兰他敏、利伐斯的明 | 痴呆症的发展 | 骨髓间充质干细胞 | 静脉输液 | 抗精神病药物会增加不良事件(意外跌倒、认知能力下降)的发生率。 |
| 沮丧 | 认知行为疗法、普拉克索、重复经颅磁刺激、文拉法辛 | 60岁以上患者服用西酞普兰超过20毫克时,QT间期延长。 | 神经干细胞 | 静脉输液 | 舍曲林、帕罗西汀、氟西汀、西酞普兰可能出现轻微不良反应,但与单胺氧化酶B抑制剂(MAO-B1)合用有禁忌。建议进行心电图监测。
海马/神经干细胞神经发生化合物NSI-189 |
| 精神病 | 氯氮平、匹莫范色林 | – | UC-MSC | 静脉输液 | 需要定期进行血液常规监测。 |
| 冲动控制障碍 | 认知行为疗法 | – | – | – | 应监测多巴胺激动剂戒断综合征。 |
| 漠不关心 | 吡贝地尔 | 合并抑郁症,照护者负担 | – | – | 监测接受丘脑底核深部脑刺激手术后患者的冷漠症状 |
| 体位性低血压 | 多巴酚丁胺、氟氢可的松、米多君 | – | – | – | 适度使用利尿剂、抗抑郁药等。 |
| 慢性便秘 | 聚乙二醇、益生菌/益生元纤维 | – | 粪便微生物移植 | 经鼻肠管进入上消化道 | 益生菌补充剂对肠道菌群的影响[ 8 ] |
| 厌食、恶心、呕吐 | 多潘立酮 | – | – | – | 需要监测心电图。 |
| 唾液分泌 | 超声引导下A/B型肉毒杆菌毒素注射至腮腺/颌下腺 | – | – | – | 咀嚼 |
| 泌尿功能障碍 | 索利那辛 | – | 成肌细胞 | 括约肌内注射 | 抗胆碱能(口干、便秘)和非胆碱能(消化不良、头晕、头痛)不良反应 |
| 勃起功能障碍 | 西地那非 | – | ASC | 静脉输液 | 监测体位性低血压 |
| 失眠 | 金刚烷胺、艾司佐匹克隆、褪黑素 | – | – | – | 适度使用抗帕金森病药物;持续气道正压通气治疗阻塞性睡眠呼吸暂停;进一步调节肠脑轴(肠道菌群中添加发酵乳杆菌PS150) |
| RBD | 氯硝西泮,褪黑素 | – | – | – | 适量使用SSRIs、SNRIs、TCAs、MAO-BI 或苯二氮卓类药物 |
| 疼痛 | 阿片类药物 | – | – | – | 监测便秘、肠道菌群(可通过益生菌补充剂和间充质干细胞来源的外泌体注射进行调节) |
| 疲劳 | 雷沙吉兰 | – | – | – | – |
表1 神经精神疾病及早期帕金森病/帕金森病前期治疗
对于帕金森病(PD)引起的焦虑和抑郁等神经精神症状,选择性血清素再摄取抑制剂(SSRIs)/抗抑郁药(获准用于治疗焦虑、抑郁和其他情绪障碍)包括西酞普兰(Celexa)、艾司西酞普兰(Lexapro)、氟西汀(Prozac)、氟伏沙明(Luvox、Luvox CR)、帕罗西汀(Paxil、Paxil CR)、舍曲林(Zoloft)和维拉唑酮(Viibryd)。在帕金森病治疗抑郁症(由于大脑中产生多巴胺、去甲肾上腺素或血清素的区域功能失调)时,SSRIs可能会加重5%至20%帕金森病患者的震颤。阿米替林虽然临床上被认为有效,但其抗胆碱能副作用会引起心律失常或认知功能下降,因此根据指南,应特别注意其在治疗此类疾病时的作用。对于患有高血压和/或糖尿病的帕金森病患者,也有必要预防和治疗脑血管疾病相关的认知障碍(表2 )。
| 潜在的生物疗法干预 | 研究设计信息 | ||
|---|---|---|---|
| 细胞来源 | 配送路径 | 治疗次数/检查项目 | 报告年份 |
| 胚胎多巴胺细胞 | 植牙手术 | 共34例/(NCT00038116) | 2001–2009 |
| 胚胎干细胞来源的A9多巴胺祖细胞 | 将壳核注入大脑(~ 10 6) | 12名患者/(NCT05887466) | 2001–2023 |
| 自体脂肪组织来源的基质血管成分 | 皮下注射(~ 10⁷) | 10名患者/炎症生物标志物在12个月随访期间(NCT05699161) | 2009–2020 |
| 胚胎干细胞衍生的神经前体细胞 | 纹状体植入 | 共50例/(NCT03119636) | 2018 |
| RC17腹侧中脑多巴胺能祖细胞 | 外科植入(10 6 –10 7 /六轨) | 8例患者/HLA I 类检测 (NCT05635409) | 1989–2020 |
| 自体周围神经移植 | 单侧植入黑质 | 8名患者/深部脑刺激疗法减少 (NCT01833364) | 2016–2018 |
| 神经干细胞 | 鼻腔给药(每周106/kg) | 12名患者/(NCT03128450) | 2013–2014 |
| 自体周围神经移植 | 将电极植入黑质、基底前脑或壳核,可联合或不联合丘脑底核深部脑刺激(STN-DBS)。 | 约70名患者/DaTscan SPECT成像评估,随访长达 24 个月 (NCT02369003) | 2005–2022 |
| 单性生殖神经干细胞 | 脑内注射至纹状体和黑质 | 12名患者/(NCT02452723) | 2016–2018 |
| 自体脂肪来源的间充质干细胞 | 静脉注射 | 约 30 名患者/(NCT04995081) | 2005–2020 |
| 骨髓来源的间充质干细胞 | 静脉注射 | 20 名患者/(NCT01446614) | 2007–2010 |
| 同种异体骨髓来源的间充质干细胞 | 输液(107/kg) | 30例/(NCT04506073) | 1996–2018 |
| 自体间充质干细胞 | 静脉介入 | 30 名患者/(NCT04146519) | 2020 |
| 自体骨髓间充质干细胞 | 静脉注射途径和鼻内途径,经下鼻甲和鼻道给药 | 约 500 名患者/(NCT02795052) | 2011–2016 |
| 局部骨髓来源的间充质干细胞组分 | 静脉注射和鼻内给药途径(14毫升和1毫升) | 约 100 名患者/(NCT03724136) | 2009–2018 |
| 自体脂肪来源组织基质血管成分 | 静脉注射(500毫升) | 约 300 名患者/(NCT03297177) | 1988–2015 |
表2 帕金森病及其他神经退行性疾病患者的代表性干细胞试验与设计研究
通过药物治疗患者帕金森病相关非运动症状(PD-NMS)的方法
针对帕金森病相关非运动症状(PD-NMS)的药物治疗,需首先识别并区分症状是疾病本身进展所致,还是由抗帕金森药物(如多巴胺能药物、抗胆碱能药等)所诱发。对于药物诱发的神经精神症状,如精神病,在调整基础抗帕金森方案后若疗效不佳,可谨慎使用小剂量喹硫平进行治疗,但需密切监测其代谢副作用。同时,为保护认知功能,应避免使用苯海索等抗胆碱能药物。对于常见的冲动控制障碍,首要处理是调整(尤其是减少)相关的多巴胺受体激动剂剂量。若患者出现淡漠,可在优化多巴胺能治疗的基础上,考虑加用利斯的明。
其次,对于自主神经功能障碍和药物引起的胃肠道反应,治疗策略侧重于药物调整与非药物措施结合。直立性低血压和慢性便秘主要通过增加水盐摄入、膳食纤维、物理方法等非药物方式管理,同时应停用或减少可能加重的药物(如抗胆碱能药)。针对左旋多巴引起的食欲减退、恶心呕吐,可通过调整服药时间(如随餐或餐后服用)来改善;若症状持续,则需进一步医疗干预。
再次,睡眠障碍和疼痛的治疗需要精确评估病因并选择针对性药物。对于日间过度嗜睡,在排除其他原因(如睡眠呼吸暂停)后,若与多巴胺能药物治疗相关,可使用莫达非尼促进觉醒。对于REM睡眠行为障碍(RBD),目前缺乏高级别证据的特效药,治疗重点是排除药物诱因并密切监测。与疾病相关的疼痛(尤其是“关期”痛),主要通过优化抗帕金森药物的方案(如调整剂量或给药频率)来延长“开期”、缩短“关期”,从而获得缓解。
最后,对于其他复杂症状,治疗需多管齐下并关注新兴疗法。泌尿功能障碍和勃起功能障碍需先排除其他常见病因。目前,自体间充质干细胞(MSC)疗法在治疗尿失禁方面显示出潜力。针对疲劳这一复杂症状,可使用专业量表(如AEIFS)进行评估,治疗需综合处理所有潜在诱因(如睡眠差、抑郁、运动症状未控等)。此外,调节肠道菌群的益生菌疗法等生物治疗新途径也正在探索中,为PD-NMS的综合管理提供了未来方向。
干细胞移植治疗改善帕金森病患者运动功能的策略
干细胞移植治疗改善帕金森病患者运动功能的策略,其核心在于利用细胞的再生与修复能力,替代或补充受损的多巴胺能神经元,并创造有利于神经修复的微环境。目前的研究焦点主要集中在对间充质干细胞(MSC),尤其是人脐带间充质干细胞(hUC-MSC)的运用。这类细胞因其来源广泛、易于扩增、免疫原性低及具有多向分化潜能等技术优势,被视为理想的细胞来源。移植策略可通过腰椎穿刺或直接脑内注射(如纹状体)等途径将细胞送达目标区域。其作用机制不仅包括分化为功能性多巴胺能神经元,还可能通过分泌神经营养因子、调节局部免疫微环境(如通过IDO、IL-10等通路抑制排斥反应)来促进宿主神经元的存活与功能恢复。
大量临床前研究和初步临床试验为这一策略的有效性提供了证据支持。在帕金森病大鼠模型中,移植hUC-MSC或其分化出的酪氨酸羟化酶(TH)阳性细胞,能长期存活、迁移,并显著改善苯丙胺诱导的旋转行为。
在人类患者中,早期研究中的另一项案例显示,8名帕金森病患者经颈动脉注射MSC,该方案已在动物模型中验证。结果显示,患者的日常生活能力、运动症状(强直、震颤)及统一帕金森病评定量表(UPDRS)评分均显著改善(cjter.com)。
另有研究报道,在38名帕金森病患者中采用蛛网膜下腔注射MSC,1个月后UPDRS评分亦显著提高,随访期间仅出现极少数不良免疫反应(部分报告称运动功能/技能在36个月后改善达80%)。
在中国,近期帕金森病干细胞临床试验已进入新阶段,重点关注认知功能、情绪心理改善及PD-NMS的干预。
为克服单纯移植细胞存活率低、功能整合有限等瓶颈,当前的研究前沿已发展到基因增强型干细胞疗法。这一策略将干细胞作为基因治疗的载体,在移植前通过基因工程手段对其进行修饰。例如,导入关键转录因子Nurr1以促进干细胞向多巴胺能神经元高效分化;或过表达酪氨酸羟化酶(TH) 基因以直接提升多巴胺的合成能力。动物实验表明,这种经基因修饰的干细胞移植后,能在宿主脑内表达更高水平的多巴胺和TH,并产生比普通干细胞移植更显著、更持久的行为学改善。此外,在移植前用多效生长因子等对细胞进行“启动”预处理,也被证明能进一步促进移植物的存活与功能。
综上所述,干细胞移植治疗帕金森病的运动功能策略,正从基础的细胞替代疗法向更复杂的综合生物治疗演进。未来的理想策略将结合优化的细胞来源(如hUC-MSC)、基因工程增强、以及可能的免疫疗法(如联合抗α-突触核蛋白抗体),以多管齐下的方式,旨在实现神经再生、阻止神经退行性变扩散并修复微环境。虽然长期疗效、对非运动症状的益处以及治疗标准化仍是需要深入研究的挑战,但现有的证据表明,这一领域已成为帕金森病极具潜力的修复性治疗方向。
干细胞治疗帕金森病的机制和生物治疗微环境及靶点
第一,通过旁分泌作用主导神经保护与修复。 移植的间充质干细胞(MSC)主要机制并非直接大量替换神经元,而是作为一个“生物工厂”,通过分泌丰富的营养因子(如BDNF、GDNF、NT-3、VEGF等)创建有利的再生微环境。这些因子发挥关键的神经营养、抗凋亡和促血管生成作用,保护残存的多巴胺能神经元,促进内源性修复,并为可能的细胞整合提供支持。这被认为是改善症状和延缓疾病进展的主要疗效来源之一。
第二,发挥强大的免疫调节与抗炎效应。 帕金森病脑内存在显著的神经炎症,表现为小胶质细胞活化及促炎因子(如TNF-α、IL-1β)水平升高。MSC能够通过细胞接触和分泌可溶性因子(如IL-10、PGE2、TGF-β1),抑制过度激活的免疫细胞,诱导抗炎的调节性T细胞,并促进促炎性α-突触核蛋白的清除。这种将病变脑部微环境从“促炎”状态调整为“抗炎/修复”状态的能力,是干细胞治疗的关键靶点和独特优势。
第三,提供细胞替代与代谢支持。 在优化条件下,部分移植细胞可分化为多巴胺能样神经元,或激活内源性神经干细胞,尝试直接补充神经元数量。更前沿的策略是通过基因工程(如过表达Nurr1、酪氨酸羟化酶TH或GDNF)增强其分化能力与治疗效果。此外,研究揭示干细胞还能通过转移正常线粒体 给受损神经元,改善其能量代谢并减轻氧化应激,从细胞代谢层面提供支持(图1)。
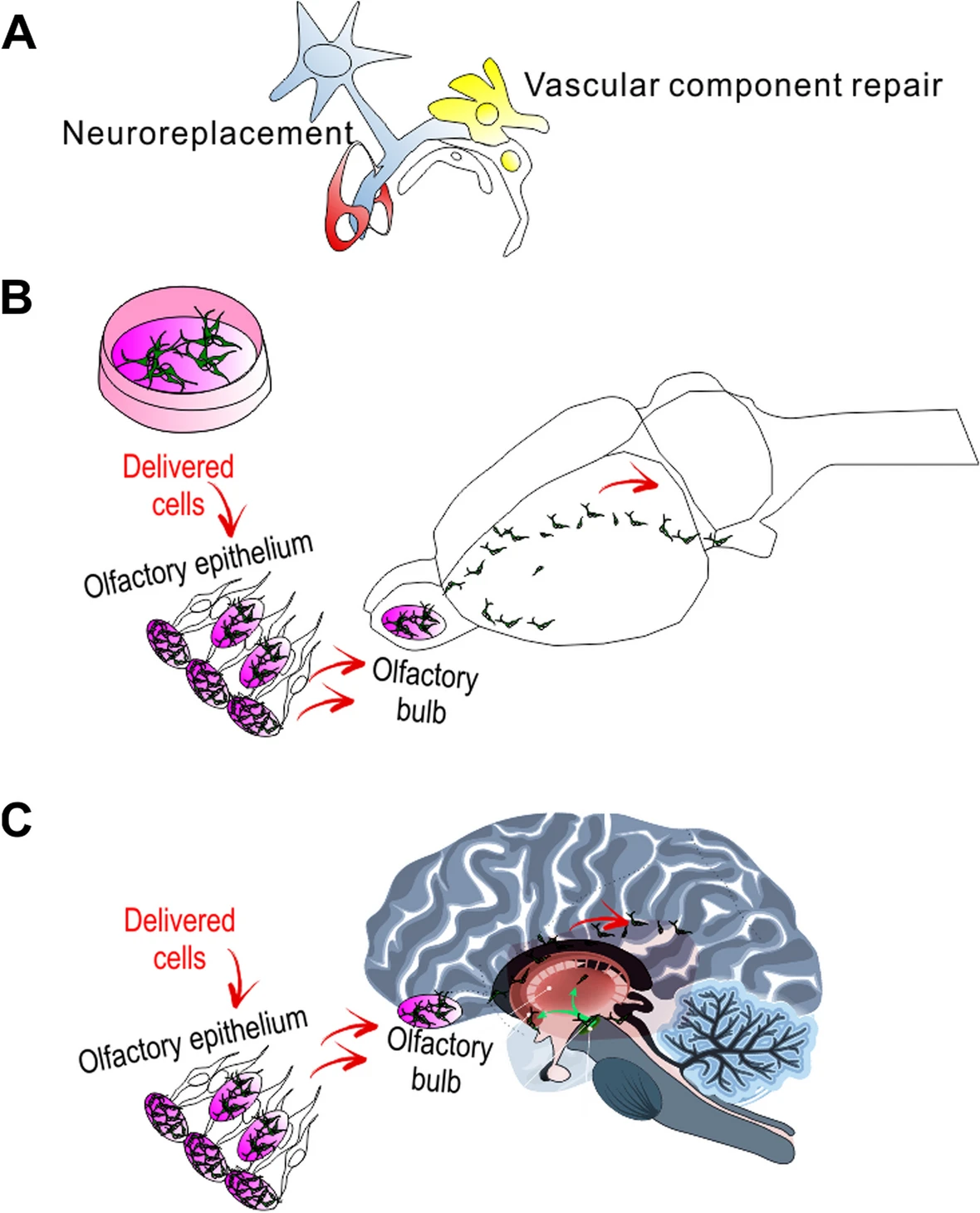
图1:细胞移植治疗示意图。移植的细胞具有发挥多种功能的潜力,它们进入大脑后,迁移至损伤部位,并转化为神经元样细胞,直接替代受损/坏死的神经元,从而保护未受损的神经。目前,基于神经保护作用的干细胞机制已有总结,但仍存在局限性。此外,间充质干细胞(MSC)具有强大的旁分泌效应,能够分泌或促进脑源性神经营养因子(BDNF)、胶质细胞源性神经营养因子(GDNF)、血管内皮生长因子(VEGF)等活性物质的产生。预期这些移植的细胞能够促进新生祖细胞的存活、增殖和分化,促进新血管的形成,迁移至损伤部位,并通过促进突触的形成来帮助激活神经回路。
第四,通过主动工程化和优化策略增强疗效。 为提高治疗效率,研究正从被动移植转向主动设计。策略包括:
- 1)细胞预处理:在移植前利用缺氧、炎症条件或生长因子(如多效生长因子)“启动”干细胞,提升其存活率与适应性;
- 2)基因增强:构建能持续表达神经营养因子或关键酶的工程化干细胞;
- 3)联合递送:使用生物材料(如PLGA微球)作为载体,协同输送细胞与神经营养因子。这些策略的核心目标是精准调控移植局部微环境,解决细胞滞留率低、存活时间短等瓶颈。
综上所述,间充质干细胞治疗帕金森病的机制是一个以 “旁分泌调控”和“免疫调节”为核心基础,辅以 “细胞替代”和“代谢支持” 潜力,并通过 “工程化策略”不断优化 的协同系统。其根本作用靶点是病变脑组织的整体微环境,旨在将其重塑为一个利于生存、修复与再生的“生态位”,从而实现对疾病多通路的综合干预。未来研究的重点在于如何标准化这些策略,并确定最佳的细胞类型、递送途径和治疗时机。
实验证据、递送途径与治疗前景
直接的实验证据支持了MSCs对NMS的疗效。在慢性应激或炎症诱导的抑郁/焦虑动物模型中,经鼻腔或海马区移植MSCs,能显著改善动物的抑郁样和焦虑样行为,并伴随海马神经发生增强和炎症因子水平下降。这些行为学与生化指标的改善,为MSCs治疗PD相关的情绪障碍提供了概念验证。
递送途径的选择显著影响治疗的侵入性与靶向性。传统的脑内注射虽定位准确但创伤大。相比之下,经鼻腔给药作为一种无创、可重复的递送方式,表现出独特优势。干细胞通过嗅神经和三叉神经通路,可绕过血脑屏障直接进入中枢神经系统,并趋向病变区域。
为了验证上述假设,我们的标准实验方案包括在鼻内移植前进行体外标记。在实验设计中,评估组接受氟西汀治疗作为阳性反应的对照治疗,然后在移植后进行动态追踪(如果使用SiPO标记的细胞进行移植,则在核磁共振(NMR)下进行追踪)。数据为细胞的保留和内源性胶质细胞/神经元的再生提供了证据。预计抗炎反应、神经元再生或其他一些分子信号通路(BDNF-TrkB-PI3K/Akt、β-catenin 和 Notch)的参与,将为抑郁症的额外益处提供机制(图2)。最新结果表明,干细胞移植可以改善宿主大脑状况,并且已被证明安全有效,可用于疼痛管理以及焦虑、抑郁、失眠或其他帕金森病前驱症状的治疗(图3)。
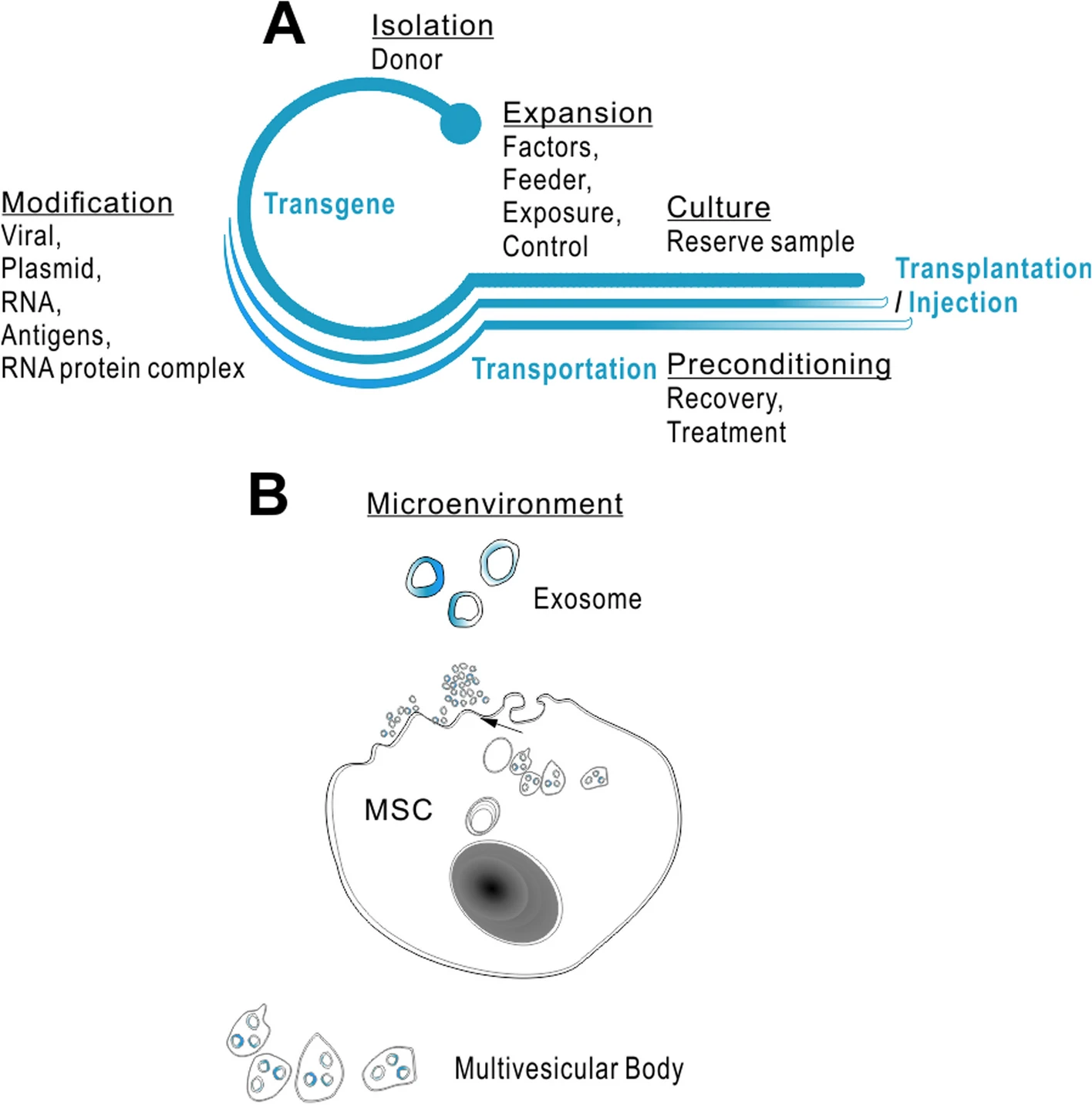
图2:干细胞通过外泌体介导微环境策略发挥作用。组织干细胞已从脂肪组织、羊水、骨髓、嗅黏膜、外周血、胎盘、脐带血和尿液中分离得到。这些干细胞的筛选标准包括多向分化能力、良好的增殖和分化能力、与生物材料的结合潜力、易于分离和培养,以及自体移植的非免疫原性。已有研究尝试总结细胞治疗后移植疗法在帕金森病(PD)治疗中的作用机制。
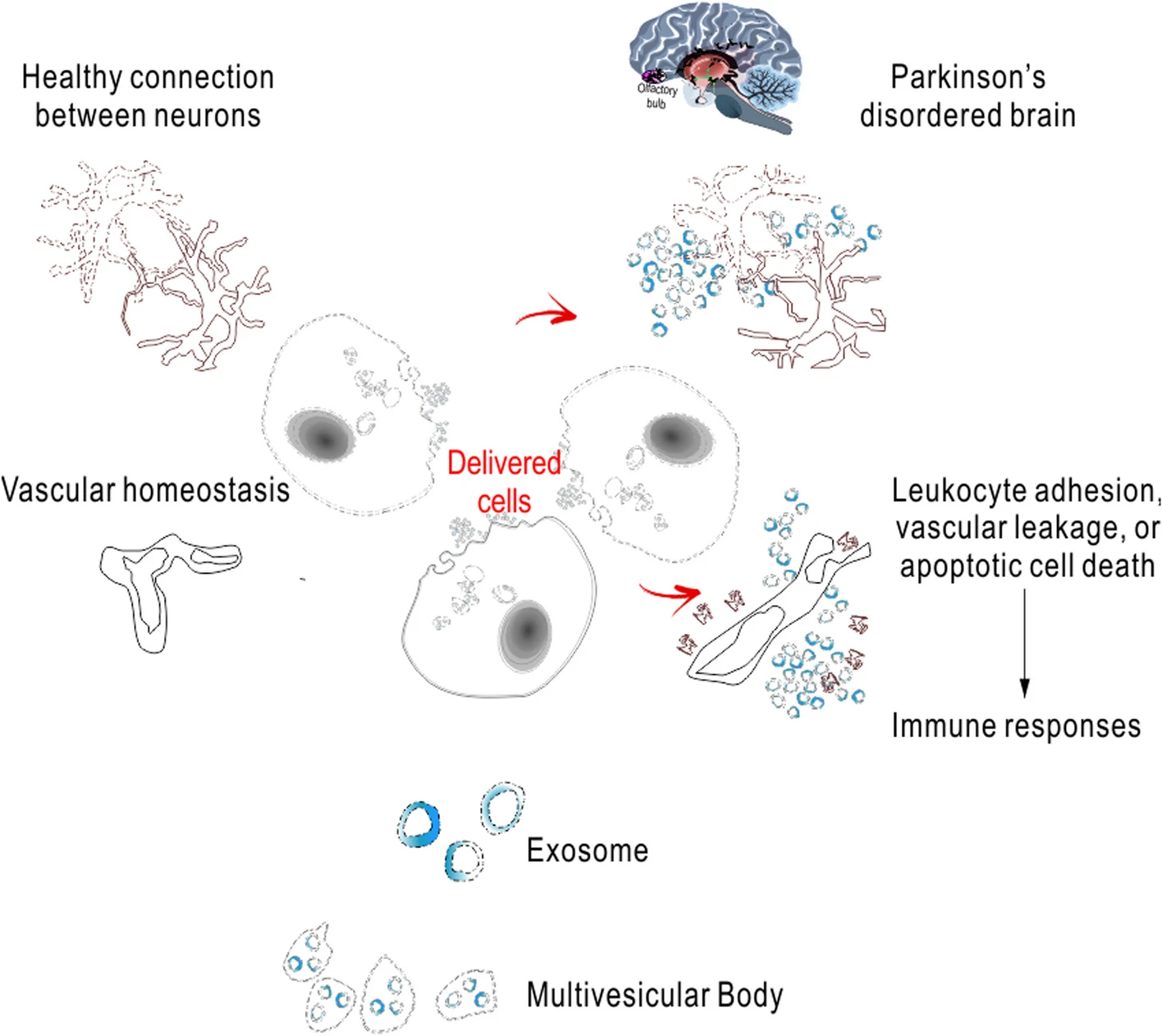
图3:生物疗法疾病修饰治疗。国际帕金森病和运动障碍协会(www.movementdisorders.org)2011年和2019年的指南中纳入了针对帕金森病非运动症状(PD-NMS)的特定治疗结果评估,并提供了其优化、推荐和标准化的治疗策略。该评估仅基于对大型PD-NMS干预候选人群的随机试验的临床意义、有效性和安全性进行。
综上所述,间充质干细胞疗法代表了一种通过多机制、多靶点重塑神经微环境的整合性治疗策略。它不仅有望改善PD的运动症状,更在缓解抑郁、焦虑、认知障碍等运动前及伴随的非运动症状方面展现出广阔前景。未来的研究重点在于优化细胞制备工艺、确定最佳治疗时间窗、开发更高效的递送系统(如使用外泌体或无细胞制剂),并通过严谨的长期临床试验验证其安全性与疗效。
结论
帕金森病的非运动症状,尤其是运动前症状,严重损害患者生活质量,且现有治疗方法存在局限。间充质干细胞治疗帕金森病主要通过其神经保护、免疫调节、促血管生成和潜在的神经营养支持等多重机制,为从根本上干预PD-NMS提供了充满希望的新途径。尽管在标准化、长期安全性和疗效验证方面仍需深入探索,但现有的临床前与初步临床证据已强烈支持,MSCs疗法有望成为未来PD综合管理中,旨在改善整体预后的重要修复性策略。
郑重声明:本文版权归原作者所有,转载文章仅为传播更多信息之目的,如作者信息标记有误,请第一时间联系我们修改或删除,多谢。

发表回复