昨天(2025年11月3日 12:40),国家慢性肾病临床医学研究中心微信公众号发布了一则关于干细胞注射液治疗糖尿病肾病的重要动态:由解放军总医院第一医学中心肾脏病医学部牵头开展的“艾米迈托赛注射液治疗糖尿病肾病患者有效性与安全性研究”项目,目前仍有入组名额,并持续面向符合条件的患者进行招募。
快讯:301医院“艾米迈托赛”干细胞注射液治疗糖尿病肾病研究继续招募中
该研究旨在评估艾米迈托赛注射液在临床进展期糖尿病肾病(DKD)患者中的治疗效果与安全性,重点关注临床进展期糖尿病肾病(DKD)患者。此项临床研究已正式获得解放军总医院伦理委员会的批准。
一、研究背景
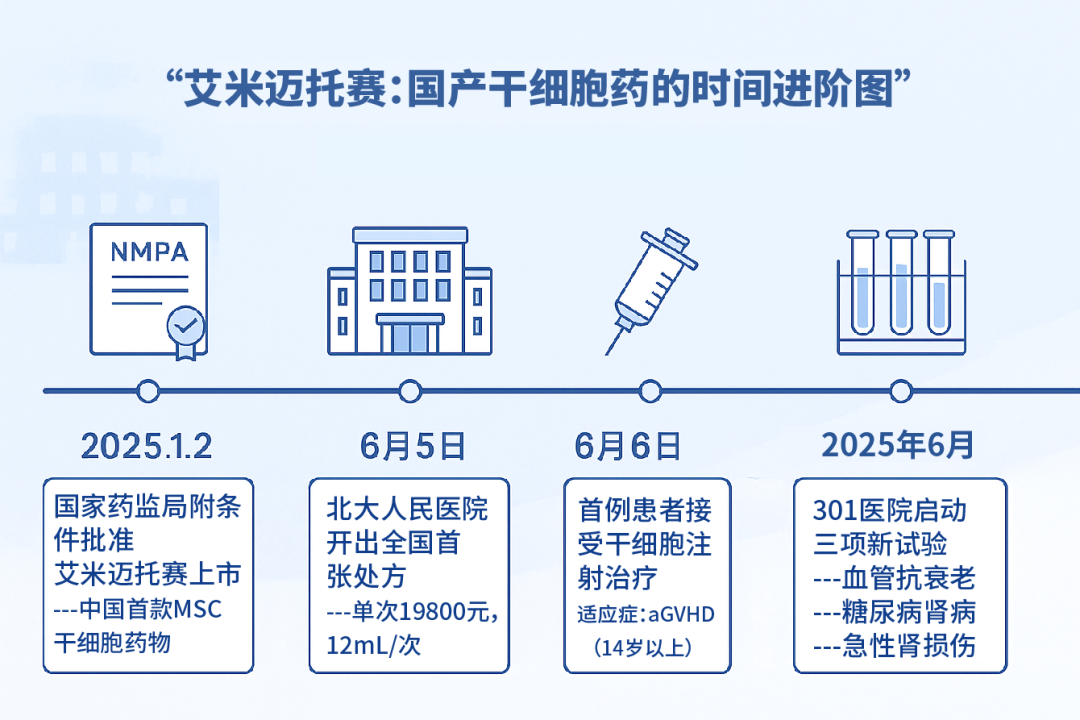
艾米迈托赛注射液,于2025年1月2日经国家药监局(NMPA)优先审评审批程序附条件批准上市,是我国首个获批上市的干细胞类治疗药物。
其主要活性成分为人脐带间充质干细胞(MSCs),可通过免疫调节、抗炎抗纤维化、促进血管生成及改善胰岛功能等机制,协同改善糖尿病相关肾损伤。
本次临床研究主要目标是:评估艾米迈托赛注射液对进展期糖尿病肾病患者的肾功能保护作用与蛋白尿改善情况;同时监测其在炎症、代谢与血管生成相关指标方面的变化;并系统评估其安全性与耐受性。

二、入选条件
符合以下基本条件者可进一步评估是否入组:
- 年龄45–80岁,男女不限;诊断为2型糖尿病;
- 10年内肾穿病理确诊糖尿病肾病;
- 24小时尿蛋白≥3.5 g,且UACR>1000 mg/g;
- eGFR≥20 ml/min/1.73m²;血压≤160/100 mmHg;
- 糖化血红蛋白<9%;签署书面知情同意书。
- 招募及筛选工作由301医院肾脏病医学部研究团队负责,最终入组资格由研究者根据医学评估决定。咨询地址:解放军总医院(301 医院)门诊大楼 6 层肾脏病医学部(周一下午、周二上午)。
三、简评
该项目由国家慢性肾病临床医学研究中心牵头,代表我国在细胞治疗糖尿病肾病领域的重要临床探索。
随着艾米迈托赛注射液的上市与应用推进,“细胞疗法+代谢病管理”的综合策略正逐步从实验室走向临床实践。
声明:本文信息来自解放军总医院第一医学中心及相关公开资料,仅供科研与医学资讯参考,不构成医疗建议。最终解释权归项目研究方所有。
郑重声明:本文版权归原作者所有,转载文章仅为传播更多信息之目的,如作者信息标记有误,请第一时间联系我们修改或删除,多谢。




发表回复