
图片来源:Elena Krivorotova / Shutterstock.com
近日,拜耳公司公布了其在帕金森病(PD)领域的两项在研疗法的重要进展。2025年9月22日,拜耳旗下临床阶段细胞治疗公司BlueRock Therapeutics LP宣布,其针对帕金森病的关键性III期临床试验exPDite-2已完成首例患者的随机化给药。该试验旨在评估其实验性细胞疗法bemdaneprocel的疗效与安全性[1]。

图源:拜耳官网截图
与此同时,由拜耳与另一家全资子公司AskBio Inc.合作开发的在研基因疗法AB-1005,其II期临床试验REGENERATE-PD也已完成首批欧洲受试者的随机化分组。这两款疗法均专注于治疗中期帕金森病,代表了拜耳在该领域的前沿探索。
这项干细胞新药的里程碑意义与专家观点
“帕金森病患者迫切需要能够改变疾病进程的新疗法,” BlueRock首席开发与医疗官Amit Rakhit医学博士表示,“exPDite-2试验的启动,是bemdaneprocel研发道路上的关键一步。我们希望在早期积极数据的基础上,继续推进这款有望恢复患者运动及非运动功能的变革性细胞疗法。”
值得一提的是,exPDite-2是首个进入关键III期临床试验的、源自异体多能干细胞的帕金森病细胞疗法。其设计基于一项包含12名受试者的I期研究结果:术后24个月内,bemdaneprocel表现出良好的耐受性,未出现与药物相关的严重不良事件,并在运动功能相关次要终点上显示出积极趋势。
基于此,exPDite-2被设计为一项多中心、双盲试验,将直接比较bemdaneprocel与假手术对照组的疗效与安全性。该试验计划招募约102名患者。

一项研究Bemdaneprocel对帕金森病成人患者的疗效和安全性的研究(exPDite-2)
其主要终点为从基线至第78周时,经16小时清醒期调整后的PD日记中“无困扰性运动障碍的开期”的增加。此外,试验还设有多项次要终点,用于评估客观运动指标、非运动症状、安全性、耐受性以及患者日常生活能力和生活质量。
拜耳制药研发负责人Christian Rommel博士补充道:“启动exPDite-2 III期试验是我们致力于变革帕金森病治疗格局的重要里程碑。bemdaneprocel的目标是持久地恢复因疾病受损的多巴胺能系统功能,从而最终改善患者的生活质量。”若本次试验结果积极,其数据将用于支持未来的上市许可申请。
疗法详解:bemdaneprocel干细胞新药如何修复帕金森病患者大脑?
Bemdaneprocel(BRT-DA01)是一种旨在替代帕金森病患者脑中丧失的多巴胺能神经元的实验性细胞疗法。其作用机制如下:
创建:BlueRock利用人类胚胎多能干细胞,在实验室中定向分化出多巴胺能神经元的前体细胞。
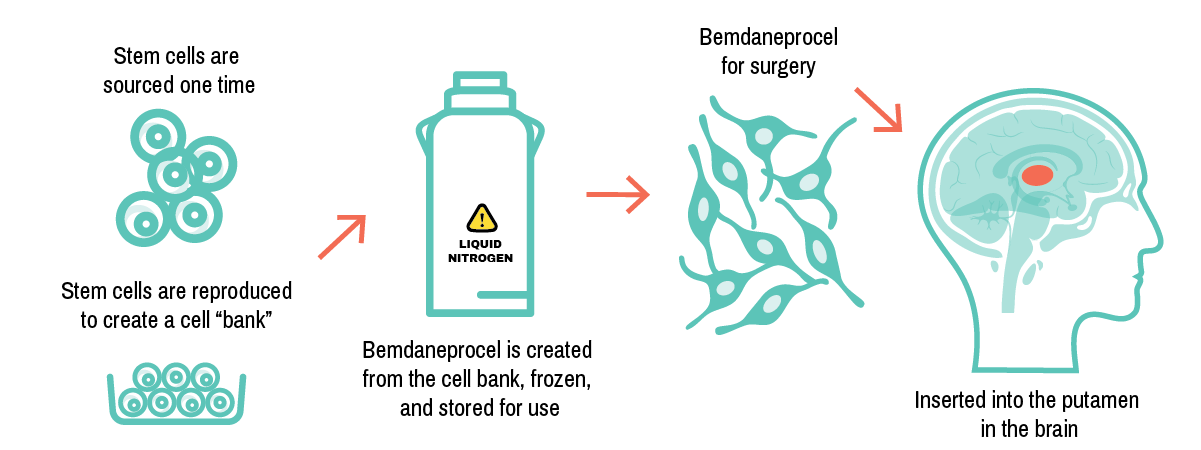
图源:expditestudy.com截图
作用:通过手术,将这些“早期形态”的细胞植入大脑的壳核区域。移植后,它们有望继续发育成熟,并重新连接被疾病破坏的神经网络,从而恢复多巴胺的生理性分泌,潜在地改善运动及非运动功能。
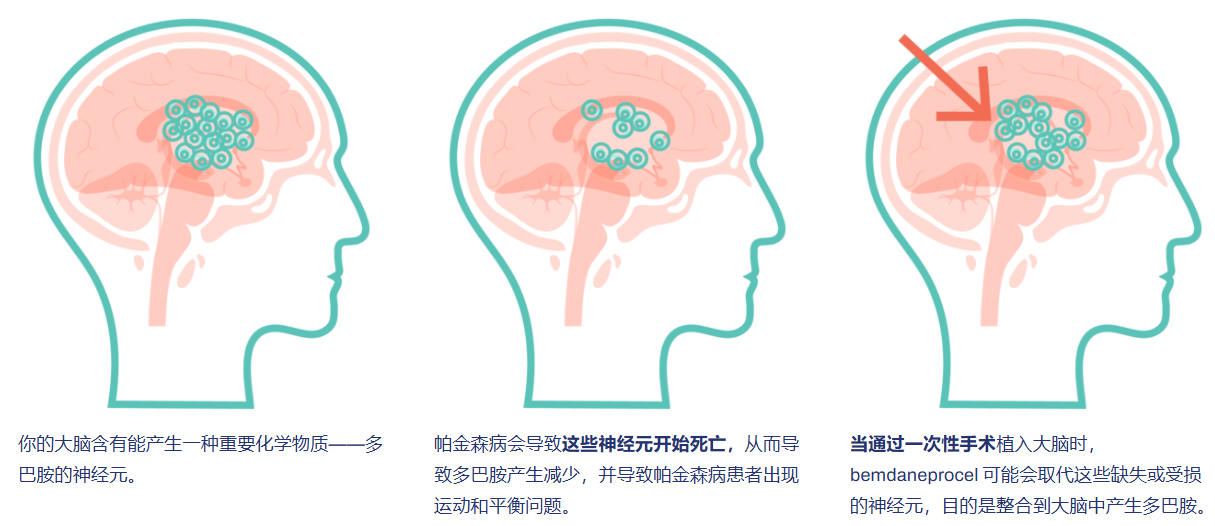
图源:expditestudy.com截图
该疗法已获得美国FDA的快速通道与再生医学先进疗法(RMAT) 资格认定,但尚未获任何监管机构批准上市。
在2024年帕金森病与运动障碍国际大会(MDS)上公布的I期临床试验数据(12名受试者)显示,术后24个月内该疗法耐受性良好,未发现与药物相关的严重不良事件。此外,在运动障碍相关的次要终点上也观察到积极趋势。这些参与者目前仍在接受长期随访研究。需要指出的是,bemdaneprocel尚未获任何卫生监管机构批准用于治疗任何疾病或医疗状况。
患者关切:谁适合?风险何在?未来何价?
目标人群: 目前试验聚焦于病程4-12年、年龄45-75岁、对左旋多巴仍有反应但出现波动的中期患者。这类患者脑中仍存有部分神经网络基础,为移植细胞的整合提供了更佳的“土壤”。
核心风险与未知: 除了脑部手术本身的风险外,最大的长期担忧在于免疫排斥(需可能长期服用免疫抑制剂)和细胞行为的不可控性(如异常增殖或形成肿瘤)。尽管I期数据良好,但更大样本和更长时间的观察至关重要。
“一次性治疗”的成本与可及性: 如果成功,这种复杂的个体化细胞疗法定价必然高昂。但其“一次性治疗、长期获益”的潜力,可能与终生服药和疾病进展带来的总医疗成本形成新的平衡。拜耳如何定价以及与医保体系的对接,将是未来影响其可及性的关键。
参加临床试验的标准是什么?
对于疗法本身,人们关心其目标人群、风险与未来。目前试验聚焦于病程4-12年、年龄45-75岁的中期患者,因其脑中仍存有可供移植细胞整合的神经网络“土壤”。除了手术风险,长期担忧主要在于免疫排斥(可能需服用抑制剂)和细胞行为的不可控性。若成功,这种一次性疗法虽定价可能高昂,但其长期获益潜力可能重塑治疗经济学。
对于希望参与试验的潜在受试者,主要入选标准包括:符合上述病程与年龄、正在接受左旋多巴治疗且每天至少有2.5小时“关期”。排除标准主要包括:曾接受深部脑刺激疗法;患有多发性硬化症、癫痫、活动性感染或近5年内有癌症病史等。
疾病背景与未来展望
帕金森病是一种进行性神经退行性疾病,对患者日常生活造成严重影响。其主要病理机制为大脑中产生多巴胺的神经细胞死亡,导致运动功能持续丧失。典型症状包括震颤、肌肉僵硬和动作迟缓。
此外,患者还常出现非运动症状,如疲劳、精力不足、认知问题和抑郁。随着时间推移,这些症状通常会不断加重,使日常活动愈发困难。
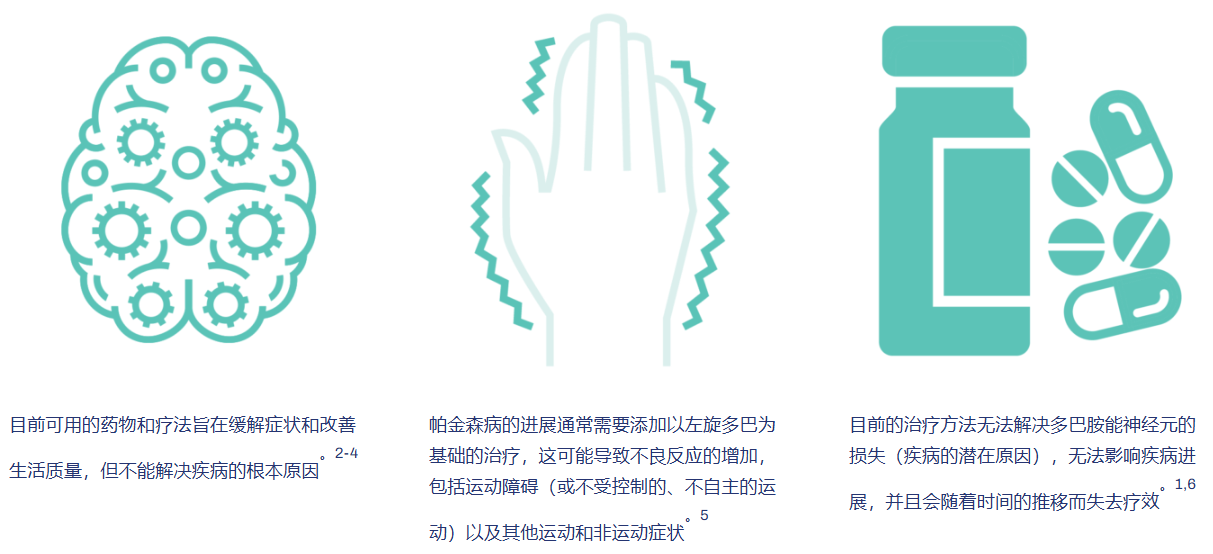
图源:expditestudy.com截图
在过去25年里,帕金森病的患病率已翻倍。目前,全球估计有超过1000万人正受其影响。这使其成为世界上第二大最常见的神经退行性疾病,也是最常见的运动障碍。至今尚无治愈方法,现有治疗手段仍不足以全面管理症状,因此对新疗法的需求十分迫切。
若III期试验成功,bemdaneprocel有望于2028年左右提交上市申请。它可能成为首个能够潜在修复帕金森病核心病理的疾病修饰疗法,实现从“管理症状”到“修复源头”的跨越,并为治疗其他神经退行性疾病开辟道路。
关于BlueRock Therapeutics LP
BlueRock Therapeutics LP是拜耳旗下一家处于临床阶段的细胞治疗公司,专注于利用细胞疗法开发针对神经系统和眼科疾病的创新药物。除bemdaneprocel外,其管线中还有用于治疗原发性光感受器疾病的OpCT-001(已进入I期临床)。 BlueRock成立于2016年,于2019年成为拜耳的全资子公司。
关于拜耳(Bayer)
拜耳是一家全球性生命科学企业,核心业务涵盖医疗健康与农业领域。公司致力于通过创新产品应对全球挑战,在2024财年拥有约93,000名员工,销售额达466亿欧元。
结语:谨慎乐观下的重要一步
首例患者给药是一个充满希望的里程碑,但III期临床试验之路依然漫长而严谨。科学探索需要耐心,对于每一位帕金森病患者及其家庭而言,bemdaneprocel所代表的“修复”理念,本身就是一束重要的曙光。我们期待未来几年,干细胞治疗帕金森病严谨的临床数据能为我们带来更明确的答案。
参考资料:
[1]:https://www.bayer.com/media/en-us/first-parkinsons-disease-patient-treatment-in-bluerocks-pivotal-phase-iii-trial-of-investigational-cell-therapy-bemdaneprocel/
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。
郑重声明:本文版权归原作者所有,转载文章仅为传播更多信息之目的,如作者信息标记有误,请第一时间联系我们修改或删除,多谢。


发表回复