近年来,我国生物医药的格局正在被干细胞技术悄然改写。一方面,间充质干细胞(MSC)凭借其多向分化和自我更新能力,在再生医学、免疫性疾病、心脑血管病、神经退行性疾病等领域不断产出新的临床数据,被视为下一代治疗手段的重要“底座”。另一方面,行业统计显示,中国的间充质干细胞新药研发管线已占全球约三成,项目密度位居世界前列。

中国6款间充质干细胞新药进入Ⅲ期临床:3款脐带源,谁将拿到下一张上市牌照?
今年1月,我国首款脐带间充质干细胞药物(艾米迈托赛注射液)的上市申请获得国家药监局受理,标志着细胞真正开始以“药物”的身份,迈向标准化临床应用。同样值得关注的是,在它身后,至少有6款MSC新药已推进至Ⅲ期或Ⅱb/Ⅲ期这一关键阶段——其中3款源自脐带,3款源自骨髓或脂肪。未来几年,干细胞药物将在哪些疾病、哪一类患者身上率先落地,很大程度上就要看这6个品种交出的临床“成绩单”。
一、6款干细胞(MSC)新药齐聚Ⅲ期
这6款药物有一个共同特征:都是异体MSC“现成药”,意味着它们可以实现标准化、规模化生产与批次放行,适应症覆盖了免疫并发症、消化道疾病、肝病和骨关节炎等重大临床方向。
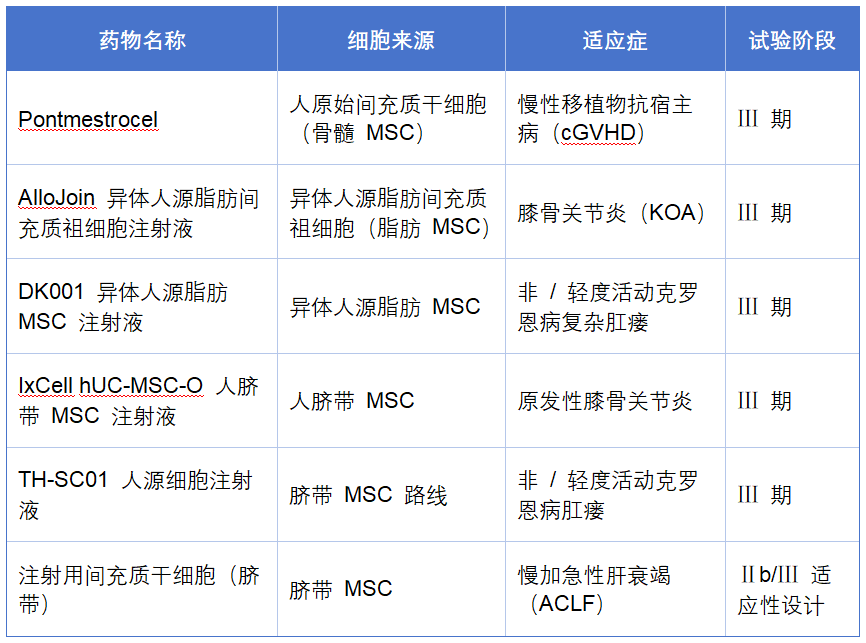
二、先看「3款脐带源」:从膝关节到肝衰竭
1)IxCell hUC-MSC-O:冲击膝骨关节炎的“保膝方案”
-
细胞来源:人脐带间充质干细胞
-
适应症:原发性膝骨关节炎(KOA),关节腔注射,Ⅲ期
-
核心价值:膝骨关节炎是典型的“大病种”,现有手段多停留在止痛、消炎和晚期的关节置换。IxCell的思路是通过脐带MSC的抑炎和改善关节微环境作用,实现“减痛+延缓疾病进展”。其Ⅱ期临床在近200例患者中已观察到疼痛和功能评分的显著改善,因此顺利进入Ⅲ期。研究显示其安全性良好,并能提供长达6至24个月的持久疼痛缓解,被许多关节科医生视为最有可能改变日常保膝路径的细胞药物。
-
细胞来源:人源MSC(脐带路线)
-
适应症:非活动性/轻度活动性克罗恩病复杂肛瘘,局部注射,Ⅲ期
-
核心价值:克罗恩病肛瘘手术复发率高且易伤及括约肌,是消化科和肛肠外科的共同难题。TH-SC01采用局部注射到瘘道周围,利用MSC的免疫调节和组织修复作用,促进瘘管闭合,同时尽力保护患者的控便功能。其III期临床试验已于2025年启动。尽管患者群体不算最庞大,但痛苦程度高、替代方案有限,加之国际上已有同类MSC产品获批,这一方向更容易获得临床与监管机构的关注。
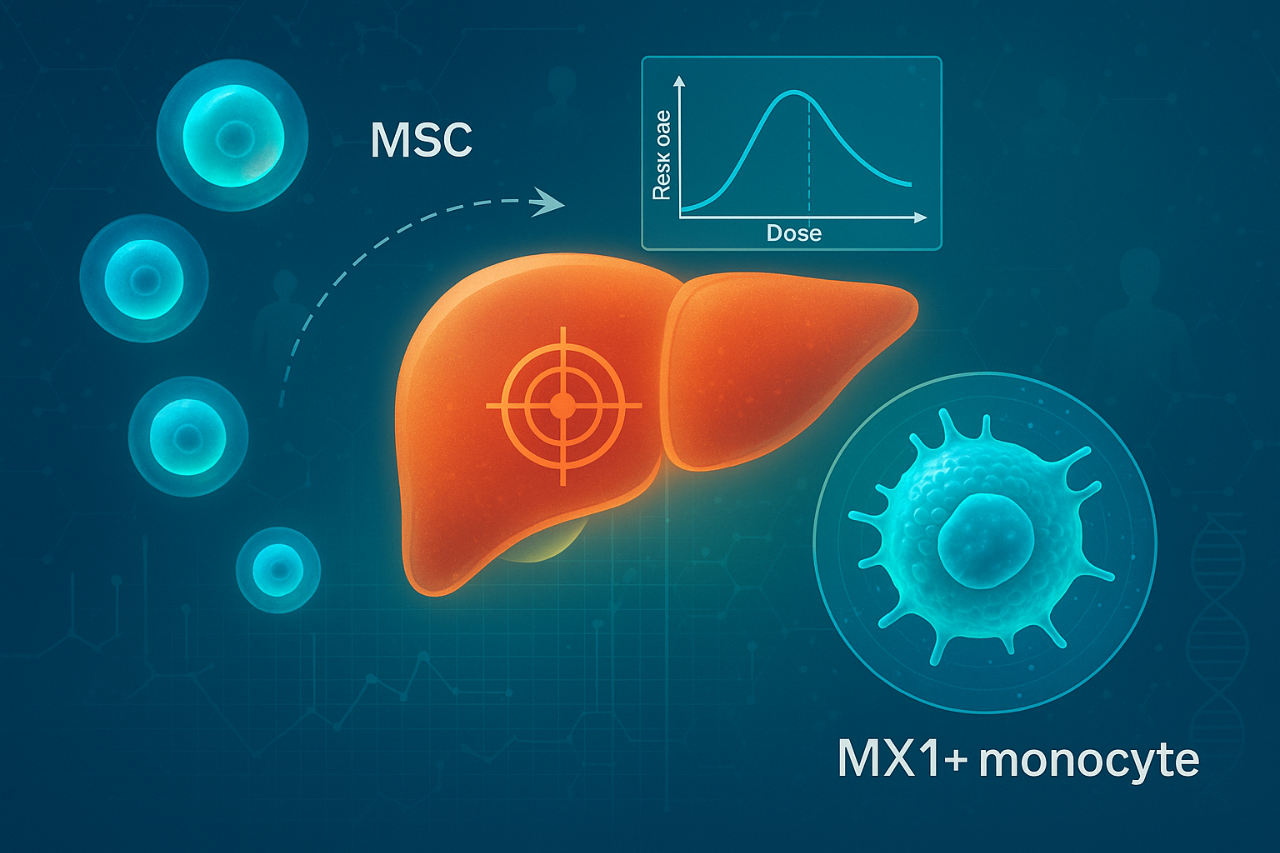
3)注射用间充质干细胞(脐带):瞄准慢加急性肝衰竭(ACLF)
-
细胞来源:人脐带MSC
-
适应症:慢加急性肝衰竭(尤其乙肝相关),静脉输注,Ⅱb/Ⅲ期适应性设计
-
核心价值:ACLF死亡率极高,许多患者仿佛“从失代偿肝硬化边缘突然跌下悬崖”。这款脐带MSC通过静脉输注,期望通过抑炎、保护残余肝细胞、调节免疫风暴,来延缓多器官衰竭,为肝脏自我修复或等待肝移植争取时间。前期研究已显示出生存率和炎症指标的改善迹象。其针对“慢加急性肝衰竭”的IIb/III期确证性临床研究已于2025年3月公示,并在4月完成首例患者入组,属于典型的“高未满足需求+高临床价值”候选药物。如果Ⅲ期能明确显示生存获益,它极有可能叩开优先审评与附条件批准的大门。
三、再看另外3款:骨髓+脂肪源的“老将”
4)Pontmestrocel:从急性到慢性GVHD的延伸
-
细胞来源:骨髓MSC
-
适应症:慢性移植物抗宿主病(cGVHD),静脉输注,Ⅲ期
-
核心价值:在急性GVHD(aGVHD)方向,中国已有脐带MSC药物(艾米迈托赛)获批。Pontmestrocel则将靶点对准了病程更长、表现更复杂的cGVHD,它同样发生在异基因造血干细胞移植之后。可以理解为:在“移植并发症”赛道上,艾米迈托赛拿到了第一张牌照,而Pontmestrocel正在争取同类适应症中的下一张。
5)AlloJoin:脂肪MSC进场挑战膝骨关节炎
-
细胞来源:异体脂肪来源MSC
-
适应症:膝骨关节炎,关节腔注射,Ⅲ期
-
核心价值:AlloJoin是国内最早进入KOA II期临床的MSC制剂之一,目前正在进行多中心Ⅲ期试验。与脐带源的IxCell相比,最大的区别在于细胞来源(脂肪 vs 脐带),这可能导致未来的制备成本、产能、长期随访安全性以及在疾病不同分期患者中的疗效差异。对患者而言,哪一款能先上市、谁在真实世界中的数据更稳定,都将直接影响未来十年的“保膝路线图”。
6)DK001:与TH-SC01正面“PK”的脂肪源选手
-
细胞来源:脂肪MSC
-
适应症:非活动性/轻度活动性克罗恩病复杂肛瘘,局部注射,Ⅲ期
-
核心价值:DK001与TH-SC01在适应症和给药方式上几乎完全对标,都是希望通过局部注射MSC来解决反复发作的克罗恩病肛瘘问题。这意味着,后续的监管审批和临床选择将会从瘘管闭合率、复发率、控便功能改善程度以及治疗成本等多个维度对二者进行比较。谁的数据更扎实、产业化路径更顺畅,谁就更有机会率先获批,或成为这一细分领域的“同类首选”。
四、三条赛道:谁最有机会率先拿证?
目前进入Ⅲ期的6款MSC新药,大致可分为三条赛道,各自的上市概率和审批节奏各不相同。
第一条是“重症救命线”:GVHD + ACLF。
这类疾病死亡率高、可选方案少,监管机构最看重的是能否带来“明确的生存获益”。Pontmestrocel针对病程更长的慢性GVHD,若能在生存率、激素减量等关键终点上跑出优势,完全符合优先审评的逻辑。而脐带MSC用于ACLF,目标是在危重患者中延长生存、改善肝功能,也属于“高未满足需求”的典型。如果Ⅲ期临床信号明确,这条线最有可能贡献出下一批获批的干细胞药物。
第二条是“慢病减负线”:膝骨关节炎。
IxCell(脐带MSC)和AlloJoin(脂肪MSC)都走关节腔注射路线,重点在于“减痛+延缓关节退变”,对全民级大病种意义重大。但KOA属于慢病,想要获批需要更大样本量和更长的随访期来证明其持续获益。虽然市场空间巨大,但上市节奏相对稳健,属于未来的“票房冠军候选”,但不一定是速度最快的。
第三条是“专病突破线”:克罗恩病复杂肛瘘。
TH-SC01和DK001正面对标,通过局部MSC注射促进瘘管闭合,改善控便功能。患者数量虽不多,但痛苦程度高,且国际上已有同类产品(如Alofisel)获批,为监管路径提供了参考。如果能在闭合率、复发率、生活质量改善上展现出全面优势,这条线极有可能出现“小而硬”的突破性品种。

五、冲刺之后:干细胞药物面临的产业化共同挑战
无论上述6款新药谁先撞线,中国干细胞药物产业在“首发上市”之后,正共同面对从“成功研发”到“成功产品”的跨越。当前,行业仍面临几大共性瓶颈:
-
细胞异质性:传统的MSC是混合细胞群,不同供体、不同批次产品间的疗效可能存在波动,这是导致临床疗效不一致的核心原因之一。
-
规模化生产:如何在不改变细胞特性与功能的前提下,进行稳定、可控的大规模扩增,是降低成本和保证市场供应的关键。
-
体内存活与功能:移植后的细胞能否在目标组织器官的复杂微环境中存活并有效发挥功能,直接影响最终疗效。
针对这些挑战,行业已在积极探索解决方案,例如开发精准亚型MSC(如三有利康的CD146+ MSC已获批IND)、优化细胞递送技术等。因此,下一阶段的竞争不仅是临床推进速度的比拼,更是生产工艺、质量控制与成本效益的综合较量。
结语
之所以是这6款药物站在Ⅲ期临床的门口,是因为它们已经跨过了干细胞“成药化”的关键门槛:安全性基本可控、制备和质控可标准化、Ⅱ期临床显示出明确的有效性信号,并且具备了开展多中心大样本Ⅲ期临床试验的能力。
接下来,它们的临床数据,将在很大程度上决定——干细胞药物会率先在哪些疾病、哪类患者身上真正落地。从首款干细胞药获得受理,到这6款MSC药物集体冲刺Ⅲ期,中国干细胞治疗的讨论,正在从“技术是否可行”,转变为“何时可用、对谁最合适”。
未来几年,当我们再提及膝骨关节炎、肝衰竭、克罗恩病肛瘘时,很可能都会多问一句:“这类病,现在有没有细胞药可以选?”而答案,正藏在这6款Ⅲ期干细胞新药的后续进展里。
郑重声明:本文版权归原作者所有,转载文章仅为传播更多信息之目的,如作者信息标记有误,请第一时间联系我们修改或删除,多谢。


发表回复